|
|
第二章化学键化学反应规律
第三节化学反应的快慢和限度
第一课时化学反应的快慢

本课时是教材第二章第三节第一课时的内容,该课时主要研究化学反应的快慢问题。第一要研究化学反应速率的概念、表示方式和计算方式,第二通过实验探究研究影响化学反应速率的因素,明确调控化学反应速率的意义。在之前的学习中,学生已经知道了化学反应有快有慢,可以通过一些宏观特征定性的表示反应的快慢,但是对于如何定量的衡量和比较不同反应的快慢问题还没有形成系统的概念。通过本课时的学习,学生可以更好地认识化学反应的快慢问题,会通过化学反应速率去计算和比较反应快慢,更好地通过外界条件去调控化学反应快慢,为今后化学反应的利用打下坚实的基础。

宏观辨识与微观探析:从宏观方面,能通过一些特殊的实验现象定性辨别化学反应的快慢,或者通过化学反应速率这个物理量来定量表示和比较化学反应快慢;在微观层面,可以通过物质结构等解释化学反应的快慢和外界因素是如何影响化学反应快慢的。
科学探究与创新意识:通过实验探究,知道反应物的温度、反应物的浓度、反应物之间的接触面积和催化剂等外界条件对化学反应速率的影响。
科学精神与社会责任:通过举例,知道在生产和生活中需要加快或者延缓某些化学反应快慢,明白调控化学反应速率具有十分重要的意义。

化学反应速率的计算和外界条件对化学反应速率的影响

学生预习本课内容;教师准备多媒体课件。

【引入】阅读教材“联想质疑”思考,在利用化学反应时,我们除了关注化学反应的物质变化和能量变化外,还应关注那些方面的问题?
学生:反应快慢和程度
【投影】生活中反应快慢不同的图片,认识化学反应的快慢
教师:这节课我们就一起学习——化学反应的快慢。
【板书】2.3.1 化学反应的快慢
【交流研讨】不同化学反应进行的快慢差别很大,在科学研究中,如何描述一个反应进行的快慢?
【学生活动】根据所学反应和知识,回答上述问题。
①冒气泡快慢
②颜色变化快慢
③固体物质的减少快慢
④出现浑浊的快慢
⑤温度变化等
【过渡】上述这些描述和比较都是从宏观实验现象定性地去分析,那么如何定量地描述化学反应的快慢呢?我们引入了一个新的物理量——化学反应速率。
【板书】 一、化学反应速率
【投影讲解】
1.定义:用单位时间内某反应物浓度的减少量(绝对值)或生成物浓度的增加量来表示。
对于一体积固定的容器中进行的化学反应:aA+bB==cC+dD
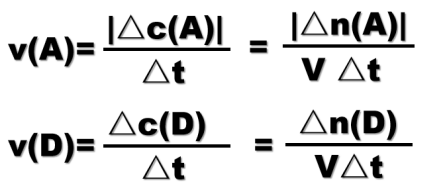 2.计算公式
2.计算公式
3.单位:mol·L-1·s-1或 mol·L-1·min-1
【讲解】化学反应速率是用来描述化学反应快慢的物理量。是使用浓度变化量与时间变化量的比值进行定义的,对于反应物因其浓度变化是一个负值,所以要取绝对值进行计算。因为c=n/V,所以,公式还可以进一步变形。根据化学反应速率公式进行计算是考查的一个重点。
【应用指导】在2L的密闭容器中,加入1molN2和3molH2,发生 N2+3H2⇌ 2NH3 ,在2s末时,测得容器中含有0.4mol的NH3,求用氮气表示的该反应的化学反应速率。
【讲解】“三段法”指的是起始、变化、终态三段。可以用物质的量浓度去表示,也可以用物质的量去表示。其中,“变化”这一段反应的物质的量或物质的量浓度与方程式中物质前面的系数成正比。
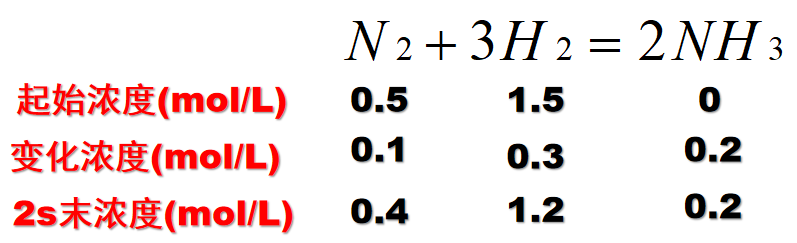 【板书】
【板书】
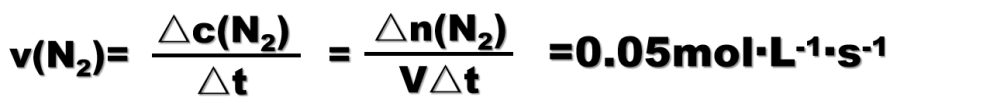
【小结】“三段法”解题思路在解有关化学反应速率的题目时,有助于理清解题思路。对以后解决化学平衡相关的题目也有很大帮助。
【思考讨论】
反应4NH3+5O2
 4NO+6H2O 在5 L的密闭容器中反应30 s后,NO增加了0.3 mol。
4NO+6H2O 在5 L的密闭容器中反应30 s后,NO增加了0.3 mol。
(1)用NO的浓度变化表示反应的反应速率为多少?
(2)用O2的浓度变化来表示此反应速率是多少?
(3)各物质的速率之比与方程式系数之比有何关系?
【学生活动】根据公式进行计算,得出结论。
(1)v(NO)=0.002 mol·L-1·s-1
(2)v(O2)=0.002 5mol·L-1·s-1
(3)各物质的速率之比等于方程式中的化学计量数之比
【归纳小结】
(1)同一个反应,用不同物质表示该反应的速率时,其数值不一定相同,但意义相同。
(2)同一个化学反应,各物质的化学反应速率的数值之比等于化学方程式中各物质的系数之比。
(3)指的是平均反应速率,不是瞬时反应速率。
(4)化学反应速率表示的是气体或溶液中溶质的反应速率,固体和纯液体的浓度是常数,所以不用来表示化学反应速率。
【迁移应用】对于反应4NH3+5O2
 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(单位皆为mol·L—1·min—1)表示,则下列式子中,正确的是
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(单位皆为mol·L—1·min—1)表示,则下列式子中,正确的是
A.
B.
C.
D.
【学生活动】根据上述所学知识,选择正确答案。 答案D。
【情景过渡】
情景一:食品添加剂是为改善食品色、香、味等品质,以及为防腐和加工工艺的需要而加入食品中的人工合成的物质或者天然物质。例如油脂抗氧化剂就是一种常见的食品添加剂。请分析油脂抗氧化剂的作用是什么?
情景二:在用煤炭或者木柴生火时,我们通常用鼓风机或扇子扇火使炉火更旺,而且如果向炉膛内加入少量的碎煤或碎木屑同样会使炉火更旺。请解释为什么会有上述现象发生?
【投影】油脂抗氧化剂图片、炉火图片
【过渡】油脂抗氧化剂是为了减缓化学反应的速度,鼓风机或扇子扇火还有加入少量的碎煤或碎木屑是为了加快炉火的燃烧,两者都对化学反应的快慢进行了人为调控。
【思考】生活中常见的化学反应,有的进行的很快,几乎瞬间即可完成,如产生美丽烟火的反应;有的进行的比较缓慢,如金属锈蚀的反应;还有一些化学反应进行的极其缓慢,如塑料降解反应。是什么原因造成化学反应速率的天差万别呢?那么我们都可以从哪些方面去调控化学反应的快慢?
【交流研讨】通过以下示例分析是哪些因素影响了化学反应速率?
(1)Na 、Mg分别与水反应时,钠与水反应更为剧烈;
(2)带火星的木条能在纯氧中复燃;
(3)新鲜水果和食物保存在冰箱里能存放得更久;
(4)实验室用H2O2制氧气时,使用二氧化锰作催化剂反应更快;
(5)木材劈得小一些烧得更快。
【学生活动】分析得出结论。
(1)物质本身性质 (2)浓度 (3)温度 (4)催化剂 (5)接触面积
【活动探究】学生阅读教材相关内容,小组合作设计实验,探究化学反应速率的影响因素
【投影】教材方法导引,并进行指导
【学生活动】实验方案设计:
1.选择化学反应
| | 2.确定待研究的影响因素
| | 3.设计改变影响因素的操作
| | 4.确定观测反应快慢的指标
| |
【学生活动】实验方案实施:根据实验结果,填写实验现象、给出结论。
实验内容
| 实验现象
| 实验结论
|

| 铁片上产生气泡速率较慢,镁片上产生气泡速率较快
| ①物质之间能否发生化学反应以及可能发生的化学反应速率的快慢是由物质本身的性质决定的
②其他条件相同时,金属越活泼,与酸反应的速率越快
|
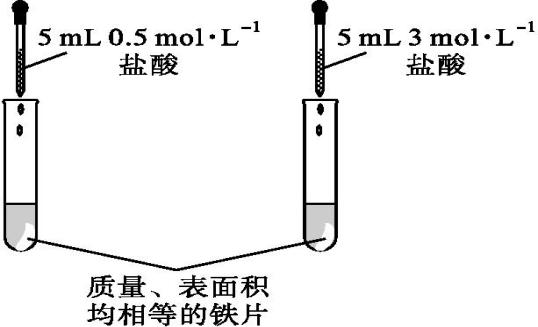
| 0.5 mol·L-1盐酸与铁反应产生气泡的速率较慢,3 mol·L-1盐酸与铁反应产生气泡的速率较快
| 其他条件相同时,反应物浓度越大,化学反应速率越快
|
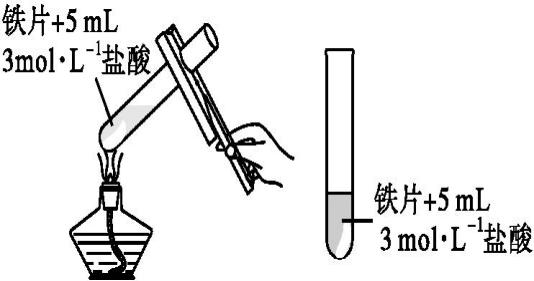
| 加热的试管中产生气泡的速率较快,不加热的试管中产生气泡的速率较慢
| 其他条件相同时,体系的温度越高,化学反应速率越快
|
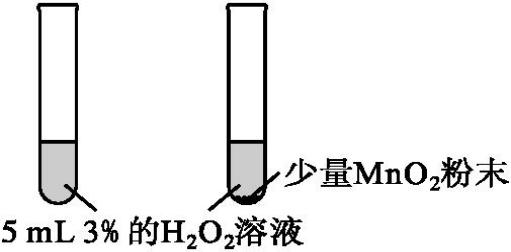
| 不加MnO2粉末的试管内无明显变化,加MnO2粉末的试管内有大量气体产生
| MnO2是H2O2分解反应的催化剂,可明显加快化学反应速率
|
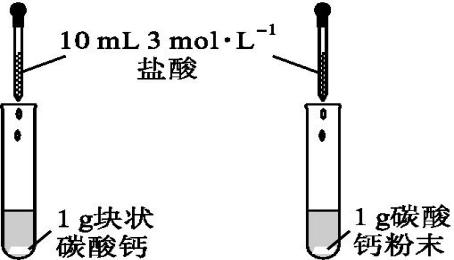
| 加碳酸钙粉末的试管内产生气泡的速率较快,加块状碳酸钙的试管内产生气泡的速率较慢
| 其他条件相同时,固体反应物表面积越大、化学反应速率越快
|
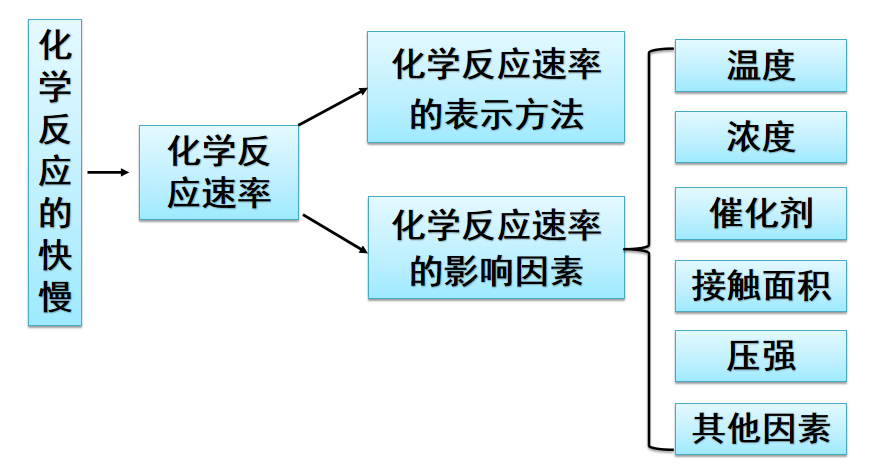
【讲解】影响化学反应速率大小的最根本原因是物质本身的性质;其他因素都是外界影响因素,比如温度、浓度、压强、催化剂、接触面积等。除了这些常见因素之外,溶剂、光波、电磁波、超声波等也可能对化学反应速率产生影响。
【板书】4.影响化学反应速率的因素
1.决定因素:反应物本身的性质
2.影响反应速率的外界因素:
【投影讲解】
(1)浓度: 其他条件不变时,增大浓度,反应速率增大
(2)温度:其他条件不变时,升高温度,反应速率增大
(3)催化剂:其他条件不变时,加入催化剂能加快反应速率。
(4)接触面积:其他条件不变时,增大反应物的接触面积可以增大反应速率
(5)压强:其他条件不变时,增大压强,反应速率增大
(6)其他因素:溶剂、光波、电磁波、超声波等。
【强调】
1.对于固体或纯液体反应物,一般情况下其浓度是常数,因此改变其量的多少,并不影响其浓度,其化学反应速率不会改变。
2.固体反应物颗粒越小,表面积越大。
3.压强变化是通过改变体积实现的,体积改变引起浓度改变,从而引起速率变化
4.压强只对有气体参与的反应速率有影响。因为压强对固体、液体的体积影响很小,对其浓度几乎无影响
【课堂小结】认识化学反应速率,探究影响化学反应速率的因素,进而对化学反应速率进行调控,是我们学习化学反应速率的重要原因。调控化学反应速率在实践中具有十分重要的意义。在生产和生活中,人们可以根据需要采取适当的措施加快某些反应过程,如钢铁冶炼、泄漏到大海里的石油的分解等;也可以根据需要延缓某些反应过程,如钢铁腐蚀、延缓塑料制品和橡胶制品的老化等。
【投影】
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图