|
|
第二章第二节化学反应与能量转化
第二课时化学电池

1.从氧化还原反应的角度认识原电池的工作原理。
2.能分析简单原电池的工作原理,能辨识原电池的构成要素。并能设计简单的原电池。

原电池的工作原理和构成要素;原电池电极材料和电解质溶液的选择。

1.根据能量变化,可将化学反应分为和。
2.破坏化学键吸收的能量大于形成化学键释放的能量的反应为反应,反应物的总能量生成物的总能量。
3.破坏化学键吸收的能量小于形成化学键释放的能量的反应为反应,反应物的总能量生成物的总能量。

二、化学反应能量转化的重要应用——化学电池
【观察思考】观察“简易氢氧燃料电池的实验”思考完成以下问题:
(1)简易氢氧燃料电池是如何将化学能转化成电能的?
(2)组装电池需要满足哪些基本条件?
氢氧燃料电池中发生的反应为:。氢分子中的氢原子在石墨电极上电子,氢气作为电池的;氧气分子中的氧原子在石墨电极上得到电子,氧气作为电池的;稀硫酸中存在的自由移动的离子起到的作用,导线起到的作用。简易氢氧燃料电池能够给用电器提供电势差,是由于在两个石墨电极上有不同的物质——氢气和氧气。
【总结】
1.原电池的基本工作原理是和分别在两个不同的区域发生氧化反应和还原反应,并通过形成闭合回路产生电流。其中,在负极上电子,是负极反应物;在正极上电子,是正极反应物;电极材料(如石墨电极)通常是。此外,还要有能传导电荷的作为离子导体;而导线则作为,起到传导电子形成闭合回路的作用。
2.原电池的构造:(1);(2);
(3);(4);
【交流研讨】生活中平常使用的 5 号电池或 7 号电池都是锌锰干电池。锌锰干电池分为酸性锌锰干电池和碱性锌锰干电池两种。酸性锌锰干电池的组成如图所示。请根据原电池原理和构造思考以下问题。
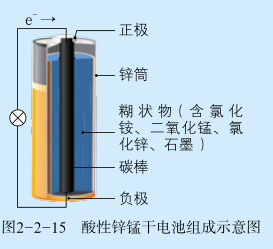
在酸性锌锰干电池中,负极反应物是,正极反应物分别是。负极材料是,正极材料是。离子导体是。
【活动探究】小组合作,根据要求设计一个简单的原电池
设计思路及依据
| 实验装置
| 实验现象
| Zn+2H+====Zn2++H2↑
| | | 确定
负极
| 选择负极反应物:_ ___
| | | | 选择负极材料:___ _
| | | 确定
正极
| 选择正极反应物:______
| | | | 选择正极材料:___________
| | | 构成闭
合回路
| 选择离子导体:____________
| | | | 选择电子导体:____
| | |
【思考】
(1)尝试分析如图 2-2-12 所示的原电池的工作原理。
锌原子电子被氧化成 Zn 2+ 进入溶液,反应式为,锌片上的电子通过导线流向铜片,溶液中的离子移向正极铜片,在铜片上电子而被还原形成氢分子逸出,反应式为。电解质溶液中 离子移向负极锌片。
(2)在如图 2-2-12 所示的装置中,锌片、铜片与稀硫酸,哪些可以替换为其他物质却同样能产生电流?
正极铜可用替换,硫酸可用替换。
【总结】3.原电池正负极材料和离子导体的选择
负极材料选择 :
正极材料选择 :
离子导体选择:
【迁移运用】根据原电池原理和设计思路,将反应Fe+CuSO4=FeSO4+Cu设计成原电池,画出装置图,并写出正负极反应式。
4.化学电池的分类:、和。
【课堂小结】
工作原理
化学电池 构成
设计方法

1.列说法中正确的是 ( )
A.原电池是把电能转化为化学能的装置
B.原电池中电子流出的一极是正极,发生氧化反应
C.原电池中电流从负极流出,从正极流入
D.原电池中的阳离子向正极移动
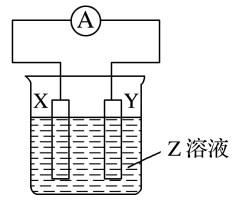
2.X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )
编号
| X
| Y
| Z
| A
| Zn
| Cu
| 稀硫酸
| B
| Cu
| Zn
| 稀硫酸
| C
| Cu
| Ag
| 硫酸铜溶液
| D
| Ag
| Zn
| 硝酸银溶液
|
3.氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如下所示。下列有关氢氧燃料电池的说法,正确的是( )
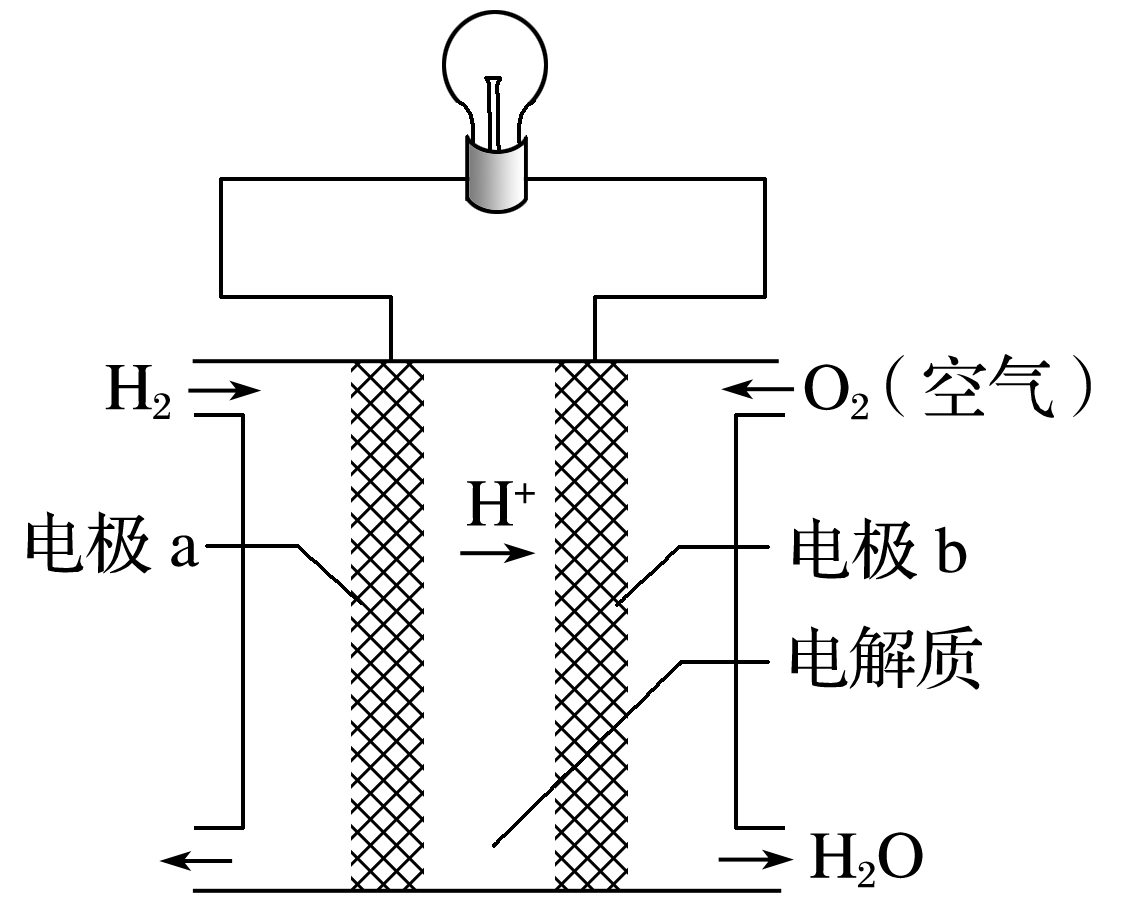
A.该电池工作时电能转化为化学能 B.该电池中电极a是正极
C.外电路中电子由电极b通过导线流向电极a D.该电池的总反应:2H2+O2===2H2O
4.如图所示电流表的指针发生偏转,同时A极的质量减小,B极上有气泡产生,C为电解质溶液,下列说法错误的是 ( )
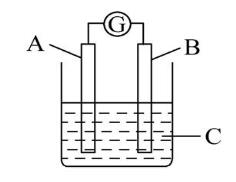
A.B极为原电池的正极 B.A、B、C分别为Zn、Cu和稀盐酸
C.C中阳离子向A极移动 D.A极发生氧化反应
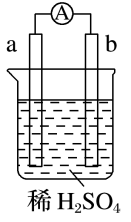 5.在如右图所示的装置中,a的金属活泼性比氢要强,b为碳棒,下列关于此装置的叙述不正确的是( )
5.在如右图所示的装置中,a的金属活泼性比氢要强,b为碳棒,下列关于此装置的叙述不正确的是( )
A.碳棒上有气体放出,溶液pH变大 B.a是正极,b是负极
C.导线中有电子流动,电子从a极到b极 D.a极上发生了氧化反应
6.将铁片和银片用导线连接置于同一稀盐酸溶液中,经过一段时间后,下列各项叙述正确的是 ( )
A.负极有Cl2逸出,正极有H2逸出 B.负极附近Cl-的浓度减小
C.正极附近Cl-的浓度逐渐增大 D.溶液中Cl-的浓度基本不变
7.下列各组材料中,不能组成原电池的是 ( )
| A
| B
| C
| D
| 两极 材料
| Zn片, 石墨
| Cu片, Ag片
| Zn片,Cu片
| Fe片, Cu片
| 插入 溶液
| H2SO4
| AgNO3 溶液
| 蔗糖溶液
| 稀盐酸
|
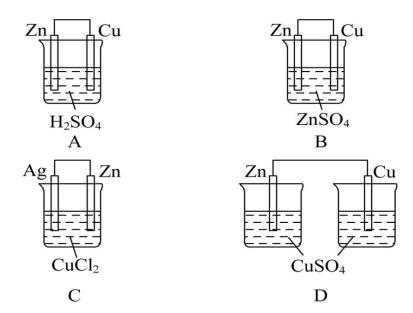
8.某原电池的总反应离子方程式为Zn+Cu2+=Zn2++Cu,则该原电池的正确组成可以是下列的 ( )
9.过量铁与少量稀硫酸反应,为了加快反应速率,但是又不影响生成氢气的总量,可以采取的措施是 ( )
A.加入适量NaCl溶液 B.加入适量的水
C.加入几滴硫酸铜溶液 D.再加入少量稀硫酸
10.氯铝电池是一种新型的燃料电池。试回答下列问题:
(1)通入Cl2(g)的电极是(填“正”或“负”)极。
(2)投入Al(s)的电极是(填“正”或“负”)极。
(3)电子从(填“Al”或“Cl”)极流向(填“正”或“负”)极。
(4)每消耗8.1 g Al(s),电路中通过的电子数目为NA(NA表示阿伏加德罗常数的值)。
检测反馈答案
1.【答案】D
【解析】原电池是把化学能转化为电能的装置;原电池中电子流出的一极是负极,发生氧化反应;电流从正极流出,从负极流入;原电池中的阳离子向正极移动,发生还原反应。
2.【答案】D
【解析】由题中所给信息(X棒变粗,Y棒变细)可知X棒是正极,Y棒是负极,金属活动性Y比X活泼,所以选项A、C均错;再看电解质溶液,B选项中硫酸里的H+在正极X棒上得电子生成氢气,X棒不会变粗;D选项中负极Y棒Zn失电子生成Zn2+,Y棒变细,Ag+在正极X棒上得电子生成Ag附着在X棒上使其变粗。
3.【答案】D
【解析】燃料电池是将化学能转化为电能,A项不正确;a极通入H2发生氧化反应,是电池的负极,B项不正确;外电路中电子由负极流向正极,即由电极a通过导线流向电极b,C项不正确。
4.【答案】C
【解析】原电池中,负极金属失去电子,发生氧化反应,溶解,质量减小,故A极为负极,B极为正极,A、D项正确;A、B、C分别为Zn、Cu和稀盐酸时,可以构成原电池,且现象符合题意,B项正确;电解质溶液中阳离子移向正极,C项错误。
5.【答案】B
【解析】显然,电极a、b与电解质溶液稀H2SO4组成原电池。因活泼性a>b(碳棒),所以a为电池的负极,b为正极。电极反应式:
a(负)极:a-ne-===an+(氧化反应)
由于正极放电消耗H+,溶液中c(H+)减小,pH增大,在外电路中,电子由a极流出经电流表流向b极。
6.【答案】D
【解析】铁片和银片用导线连接置于同一稀盐酸溶液中构成原电池,铁作负极,发生反应Fe-2e-====Fe2+,银作正极,发生反应2H++2e-====H2↑,故A错误;溶液中Cl-移向负极,负极附近Cl-的浓度增大,正极附近Cl-的浓度逐渐减小,而溶液中Cl-的浓度基本不变,B、C错误,D正确。
7.【答案】C
【解析】构成原电池的条件是活泼性不同的金属或金属和非金属,导线相连并插入电解质溶液中,则A、B、D均可以构成原电池,C中蔗糖是非电解质,故C不能构成原电池。
8.【答案】C
【解析】该原电池的负极必为锌,正极是比锌稳定的金属或导电的非金属,电解质溶液中含有Cu2+,故选C。
9.【答案】C
【解析】若加入NaCl溶液或水,会将稀硫酸稀释,c(H+)减小,反应速率减慢;若加入几滴CuSO4溶液,则发生反应Fe+Cu2+=Cu+Fe2+,析出的Cu与Fe、稀硫酸形成原电池,反应速率加快且不影响生成H2的总量;若再加入少量稀硫酸,因Fe过量,则生成H2的总量增大,且反应速率不会改变。
10.【答案】 (1)正 (2)负 (3)Al 正 (4)0.9
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图