|
|
第5课 酸和碱之间的反应
1.什么是酸碱中和
凉拌皮蛋加醋,治疗胃酸的药物


人体的酸碱平衡,土壤的酸碱性平衡


一.酸碱反应:
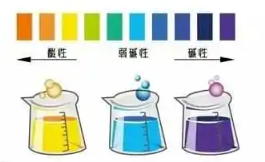
1.氢氧化钠与酸反应的实验:向盛有氢氧化钠的烧杯中滴人几滴酚酞试液,溶液变红,向变红的溶液中滴加稀盐酸,边滴边振荡,溶液颜色变浅直至消失,说明溶液由碱性变为中性或酸性,氢氧化钠和酸发生了反应。
2.实验过程中的反应方程式:HCl+NaOH = NaCl+H2O
3.实验过程与现象:酚酞无色为中性或酸性
向碱中不断滴加酸
| 颜色
| 成分分析
| 初始阶段
| 红色
| 氢氧化钠过量
| 加入少量酸
| 红色
| 氢氧化钠过量
| 加入适量稀盐酸
| 无色
| 恰好完全反应
| 加入过量稀盐酸
| 无色
| 盐酸过量
|
【实验注意】
(1)滴加盐酸需要缓慢,并且不断震荡或使用玻璃棒搅拌,使反应更充分
(2)酸与碱反应至恰好变为无色是需要保持一段时间不变色
(3)使用酚酞是因为变色明显,数据更准确
(4)操作图像如图所示
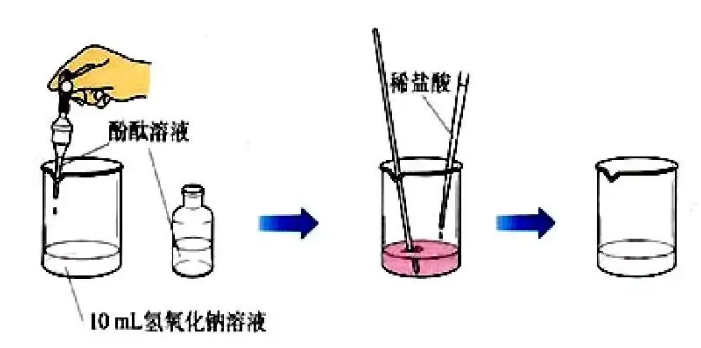
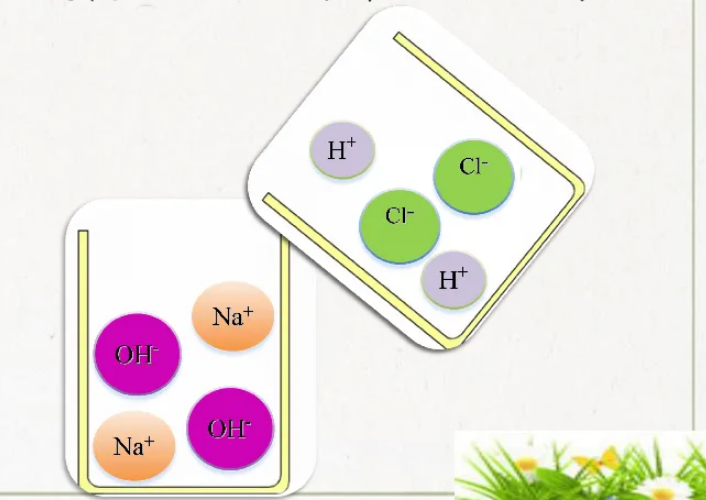
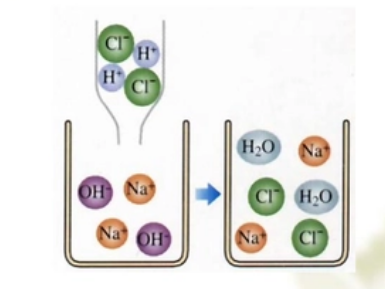
4.酸碱中和反应的实质如图所示:H++OH- = H2O
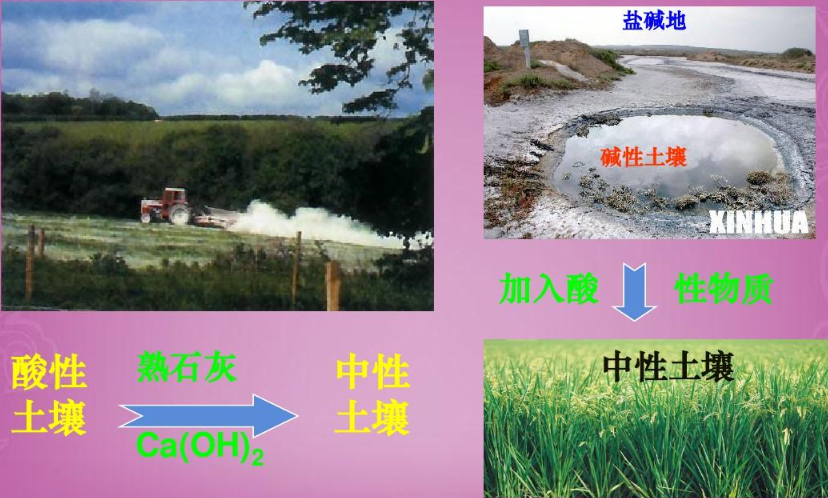
二.酸碱中和反应的应用:
1.使用熟石灰改良酸性土壤
2.使用熟石灰处理酸性的工业废水
3.精炼石油是用来中和过量的酸
三.酸碱中和反应的溶质组成成分分析:
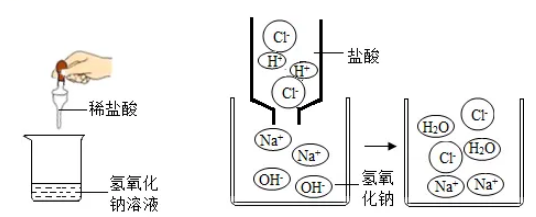
(1)未滴加酸即为氢氧化钠和水:微粒有Na+,OH-,H2O
(2)滴加少量酸即为氢氧化钠,氯化钠和水:微粒有Na+,OH-,Cl-,H2O
(3)恰好反应即为氯化钠和水:微粒有Na+,Cl-,H2O
(4)滴加过量酸即为氯化氢,氯化钠和水:微粒有Na+,H+,Cl-,H2O
1.溶液中PH的变化
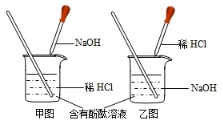
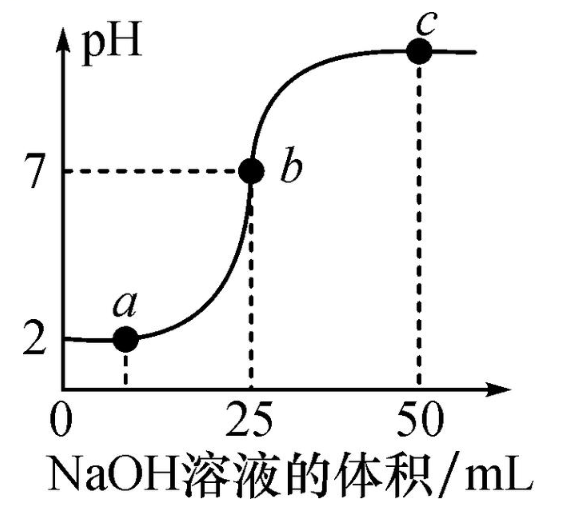
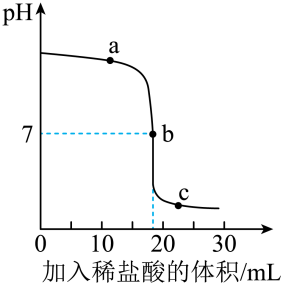
2.反应过程中温度的变化
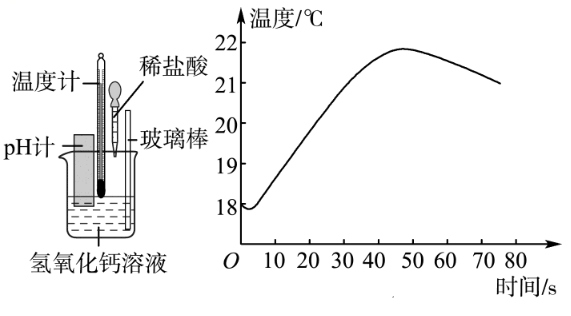
3.反应过程中电导率的变化
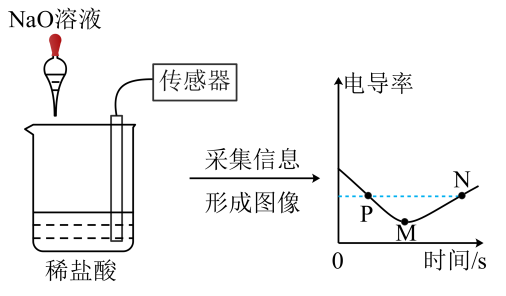
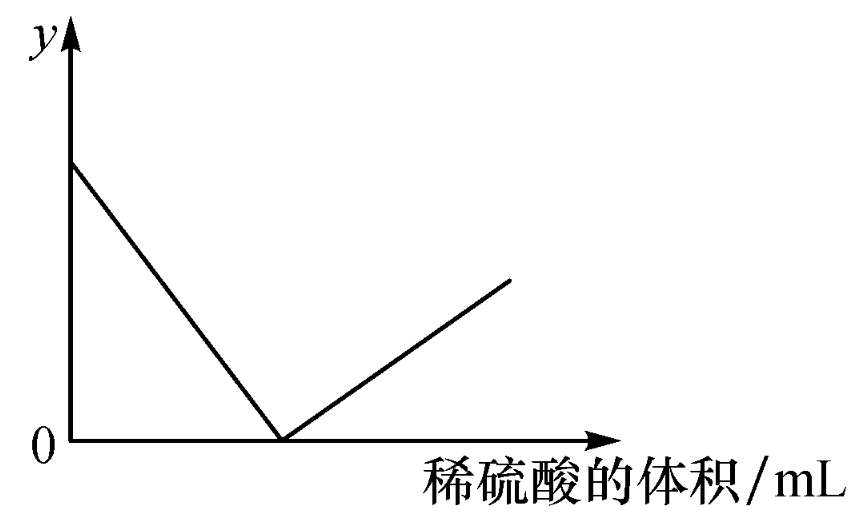
一、选择题
1.(2023·河南驻马店一模)某化学小组为探究稀硫酸和氢氧化钡溶液的反应,利用数字化实验设备测得溶液pH的变化情况如图所示。下列有关说法错误的是
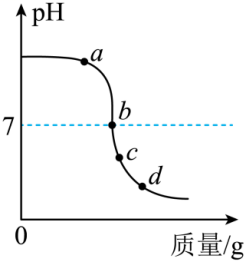
A.该实验是将稀硫酸逐滴滴入氢氧化钡溶液中
B.由a点到b点,溶液的温度升高
C.c点时,溶液中只有一种溶质
D.若将稀硫酸换为等质量、等溶质质量分数的稀盐酸,则b点右移
2.(2023·广东深圳模拟)为探究稀盐酸和氢氧化钠溶液反应过程中溶液的pH及温度随时间的变化关系,小聪同学按图甲连接好实验装置,往盛有一种溶液的烧杯中滴入另一种初始温度相同的溶液,同时用玻璃棒搅拌。图乙是数字采集器和计算机实时显示的数据曲线,下列说法错误的是
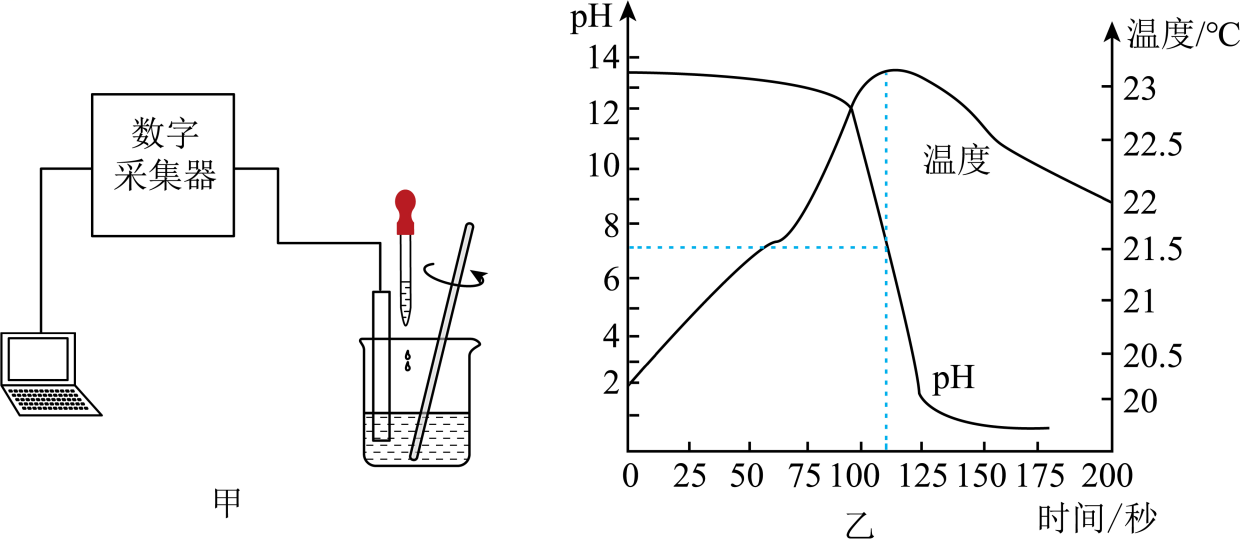
A.实验开始时,烧杯中盛有的试剂是氢氧化钠溶液 B.0~100秒时,温度上升是因为该反应放热
C.100秒时,溶液中只含有<Object: word/embeddings/oleObject1.bin>、Cl-两种微粒 D.150秒时,向溶液中加入氧化铁粉末,溶液会变黄色
3.(2023·海南海口模拟)小军向水槽中缓缓滴加稀硫酸,观察到小灯泡的亮度变化情况:亮→暗→熄→亮。下列说法正确的是
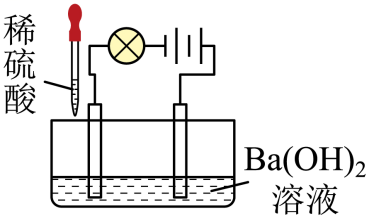
A.实验中没有白色沉淀生成
B.灯泡熄灭时,水槽中的液体中不存在粒子
C.灯泡亮度发生变化只因为溶液中的H+、OH-的浓度改变
D.将稀硫酸换成稀盐酸,观察到灯泡亮度变化不相同
4.(2023·河南周口三模)如图是酸和碱发生中和反应时的pH变化曲线。下列说法正确的是
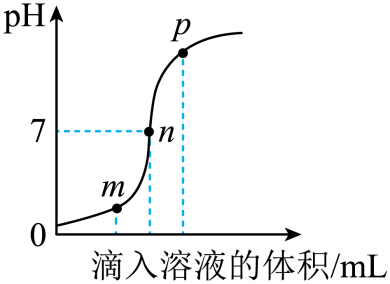
A.该反应的本质是氢离子和氢氧根离子结合生成水分子 B.该图对应的操作是将酸滴入碱溶液中
C.n点溶液的质量小于m点溶液的质量 D.向p点溶液中滴加酚酞溶液观察不到明显的实验现象
5.(2023·河南商丘模拟)如图是利用数字化传感器,测得向滴有酚酞的氢氧化钠溶液中不断滴加盐酸时<Object: word/embeddings/oleObject2.bin>的变化图像以及二者恰好完全反应的微观示意图.下列说法正确的是
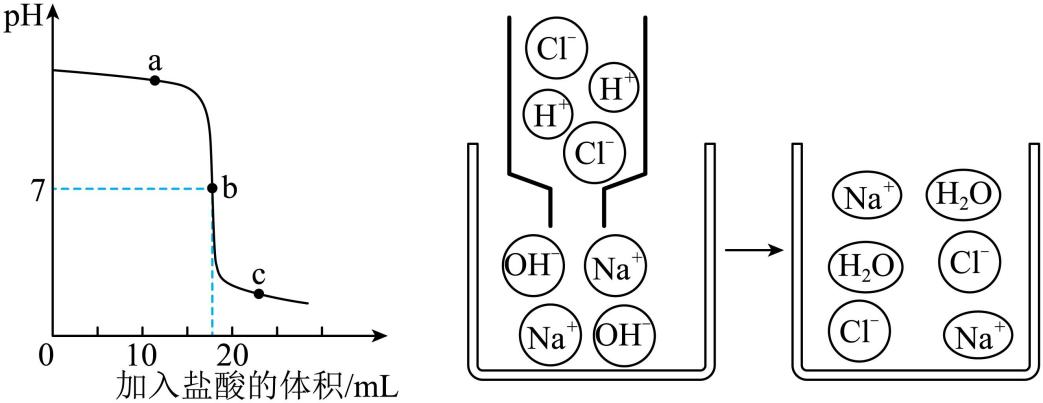
A.a点的溶质是<Object: word/embeddings/oleObject3.bin>和<Object: word/embeddings/oleObject4.bin> B.c点的溶液呈红色
C.该反应的实质是<Object: word/embeddings/oleObject5.bin> D.溶液里<Object: word/embeddings/oleObject6.bin>逐渐减少
6.(2023·陕西西安模拟)在做中和反应的实验时,小明同学向盛有一定量稀硫酸的烧杯中,逐滴加入久置的NaOH溶液,烧杯内溶液的总质量与加入溶液质量的变化趋势如图所示。下列有关说法不正确的是
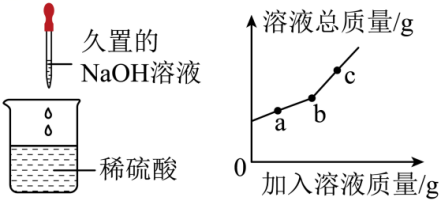
A.a~b段可观察到有气泡产生 B.a点处溶液中溶质可能有3种
C.a、b、c三点处溶液的pH依次增大 D.该NaOH溶液可能完全变质
7.(2023·福建宁德三模)为了探究稀盐酸和氢氧化钠溶液是否发生化学反应,某同学设计了图1所示装置进行实验,将一种溶液缓慢滴入另一种溶液中,测得溶液温度变化数据如图2所示。下列说法正确的是
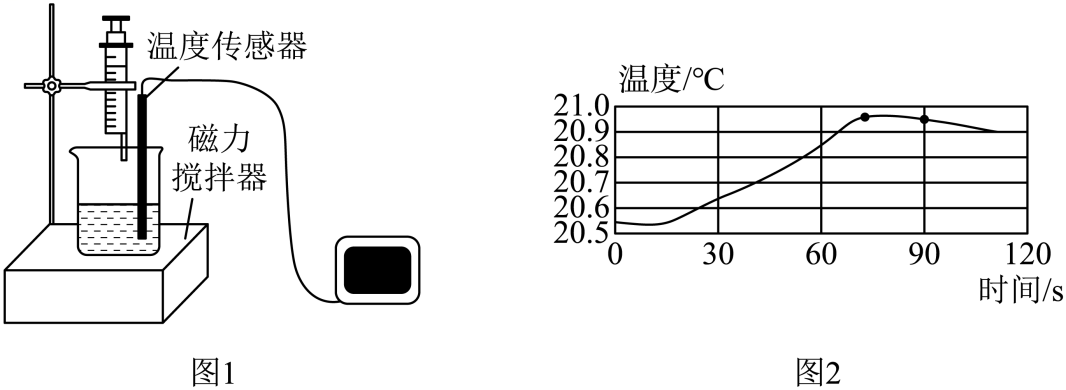
A.磁力搅拌器的作用是使溶液温度升高 B.该实验是将氢氧化钠溶液滴入稀盐酸中
C.90s时溶液中溶质只有氯化钠 D.如用pH传感器代替温度传感器也能达到实验目的
8.(2023·福建宁德三模)某兴趣小组取三份相同体积相同浓度的氢氧化钠溶液,分别滴入两滴无色酚酞溶液,再以相同的速度同时滴加不同浓度的盐酸,得到溶液的pH随时间变化的曲线如图所示。下列说法正确的是
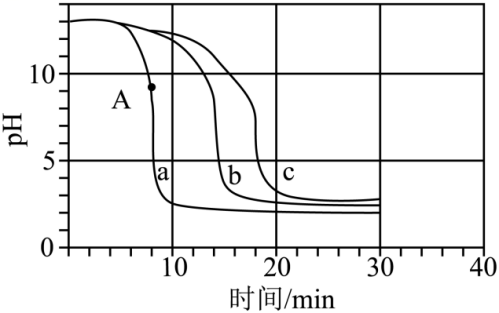
A.在a、b、c三种曲线所示的实验中,所用盐酸的浓度由大到小的顺序为<Object: word/embeddings/oleObject7.bin>
B.在a曲线所示的实验中,图中A点所示溶液中,所含的溶质只有NaOH
C.在a、b、c三种曲线所示的实验中,溶液红色最先褪去的是c
D.在a、b、c三种曲线所示的实验中,20min时溶液的酸性由强到弱的顺序是<Object: word/embeddings/oleObject8.bin>
9.(2023·湖南长沙一模)化学与生活息息相关。日常生活中的下列说法或做法不正确的是
A.浓硫酸不慎沾在皮肤上,先用大量水冲洗,再涂上3%—5%的烧碱溶液 B.氢氧化钠可作炉具清洁剂
C.被蚊虫叮咬后可涂抹肥皂水来消除痛痒 D.用熟石灰改良酸性土壤
10.(2023·山东菏泽二模)用稀硫酸与氢氧化钠溶液反应探究中和反应实验时,测得溶液pH及溶液温度的变化如图所示。下列说法错误的是
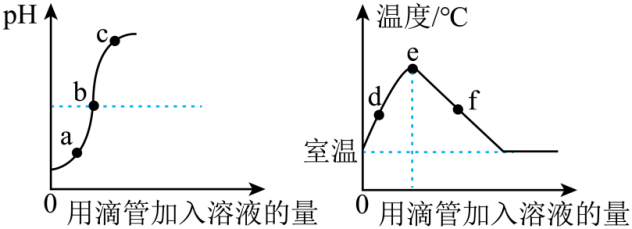
A.b点和e点表示酸碱恰好完全反应
B.该实验是将稀硫酸逐滴滴入氢氧化钠溶液中
C.图中温度曲线从室温上升到e点,说明该反应放出热量
D.f点所示溶液pH>7,能使无色酚酞试液变成红色
11.向一定量的氢氧化钠溶液中逐滴加入稀硫酸,溶液中氢氧化钠的质量、水的质量、硫酸钠的质量的稀硫酸的质量的变化关系如图所示。下列说法不正确的是
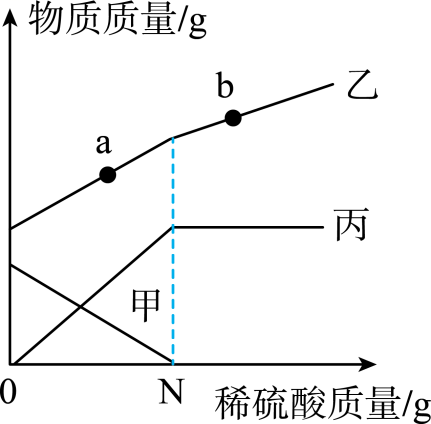
A.甲代表氢氧化钠的质量,乙代表水的质量 B.加入<Object: word/embeddings/oleObject9.bin>稀硫酸时,两者恰好完全反应
C.b点对应的溶液中含有的阳离子只有<Object: word/embeddings/oleObject10.bin> D.<Object: word/embeddings/oleObject11.bin>点对应的溶液中含有三种溶质
12.(2023·河南郑州二模)盐酸与氢氧化钠溶液反应时溶液pH的变化如下图。下列说法正确的是
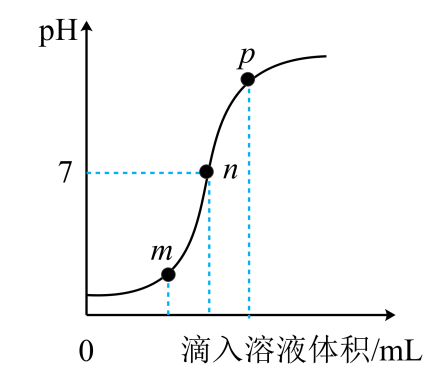
A.<Object: word/embeddings/oleObject12.bin>点所示溶液中的溶质为<Object: word/embeddings/oleObject13.bin> B.<Object: word/embeddings/oleObject14.bin>、<Object: word/embeddings/oleObject15.bin>点所示溶液中加酚酞溶液显红色
C.该图所对应操作是将盐酸滴入氢氧化钠溶液中 D.该反应的本质是溶液中的<Object: word/embeddings/oleObject16.bin>与<Object: word/embeddings/oleObject17.bin>反应生成水
13.(2023·四川成都模拟)实验小组借助传感器对稀NaOH溶液与稀盐酸的反应进行研究。三颈烧瓶中盛放溶液X,用恒压漏斗匀速滴加另一种溶液,并用磁力投拌器不断搅拌。实验装置和测定结果如图。下列说法正确的是
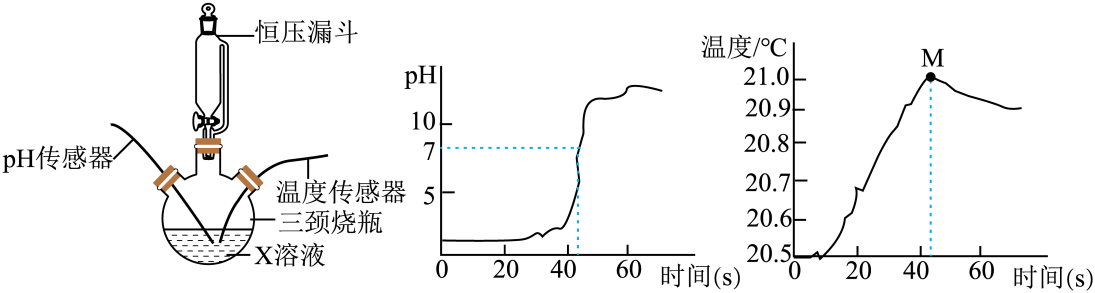
A.X溶液是稀NaOH溶液 B.0—40s溶液中H+数量不断增加
C.60s时溶液中存在离子有H+、Na+、Cl- D.温度到达M点说明两者反应放热
14.(2023·江苏苏州中考真题)常温下,将10 mL 5% NaOH溶液逐滴加入盛有5 mL 5%稀盐酸(含2滴酚酞)的锥形瓶中,边滴边振荡。下列有关说法正确的是
A.滴加过程中,锥形瓶内溶液中<Object: word/embeddings/oleObject18.bin>的数目不断增加
B.滴加过程中,溶液恰好由无色变为红色时,溶液pH为7
C.滴加过程中,锥形瓶内溶液温度不断升高
D.滴加结束后,取少量溶液蒸干,所得白色固体是NaCl
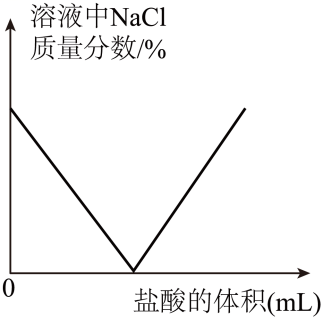
15.向一定量<Object: word/embeddings/oleObject19.bin>和<Object: word/embeddings/oleObject20.bin>的混合溶液中,逐滴加入NaOH溶液至过量,以下图像中,正确的有
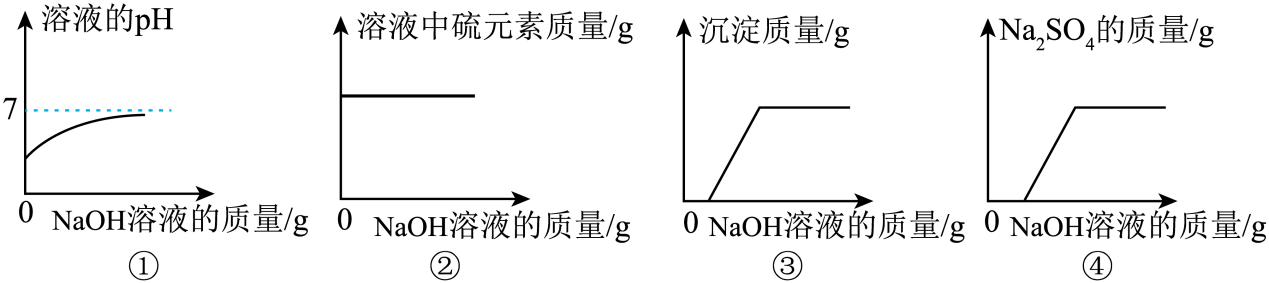
A.①② B.②③ C.③④ D.①④
16.(2023·江苏无锡二模)电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,利用数据传感技术测定溶液电导率可辅助探究复分解反应。对如图所示实验分析不正确的是
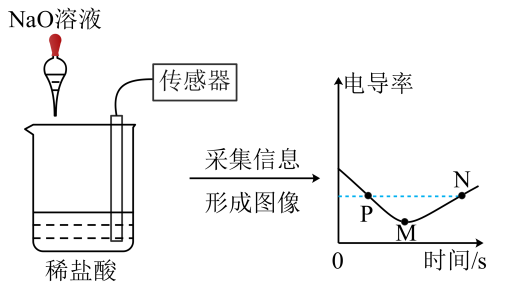
A.P点时溶液中的阳离子有Na+、H+ B.M到N时,氢氧化钠溶液过量,溶液呈碱性
C.P到M电导率减小是因为溶液中离子数量逐渐减少 D.N点时溶液中的离子数大于P点
17.(2023·河南信阳三模)向一定体积4%的氢氧化钠溶液中,逐滴加入4%的稀盐酸,有关分析错误的是
A.
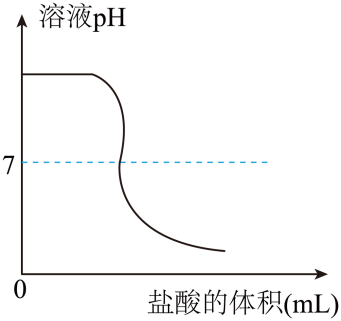 B.
B.
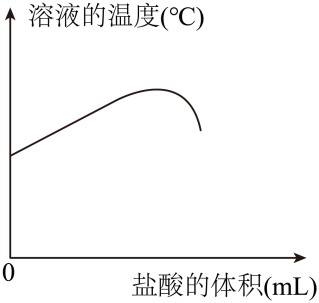 C.
C.
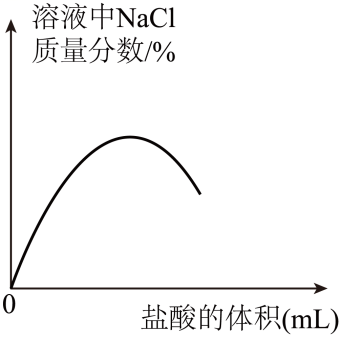 D.
D.
18.(2023·山东济南三模)某同学在常温下进行了中和反应的实验探究。向20mL0.4%的NaOH溶液(预先滴入3滴酚酞试液)中逐滴滴入0.4%的稀盐酸。利用数字化传感器借助计算机绘制出溶液pH随所滴入稀盐酸体积变化的曲线如图所示,下列有关说法中,不正确的是
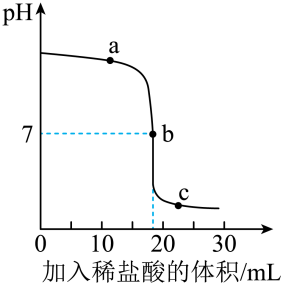
A.a点时,烧杯中溶液的pH>7 B.b点时,溶液中<Object: word/embeddings/oleObject21.bin>和<Object: word/embeddings/oleObject22.bin>恰好完全反应
C.c点时,烧杯中的溶液显红色 D.在滴入稀盐酸的过程中溶液里<Object: word/embeddings/oleObject23.bin>数目不变
19.实验室和工农业生产中,下列说法正确的是
A.氢氧化钠,碳酸钠与稀盐酸的反应都属于中和反应
B.生成盐和水的反应就是中和反应
C.中和反应的微观实质是酸溶液中的H+和碱溶液中的OH-反应生成H2O
D.中和反应都没有明显现象
20.(2021·广东中考)中和反应在生活中广泛应用,下列做法利用中和反应原理的是
A.用稀盐酸除铁锈 B.用氨水处理废水中的硫酸
C.用CaCO3作补钙剂 D.用含MgO的药物治疗胃酸过多
21.(2022秋·山东东营·九年级校联考期末)某校化学兴趣小组利用数字化传感器探究稀硫酸和氢氧化钾溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。与该实验有关的下列说法,其中不正确的有
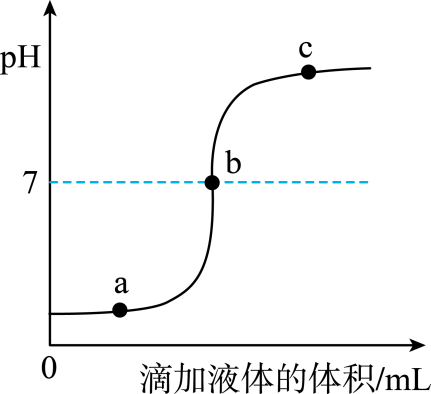
A.图中a点所示溶液中,溶质是K2SO4 B.向图中c点所示溶液中滴加无色酚酞,溶液变红色
C.该实验是向稀硫酸中逐滴滴入氢氧化钾溶液 D.b点对应的溶液中的微粒有K+,<Object: word/embeddings/oleObject24.bin>
22.(2022·四川甘孜·统考中考真题)关于右图所示实验的说法正确的是
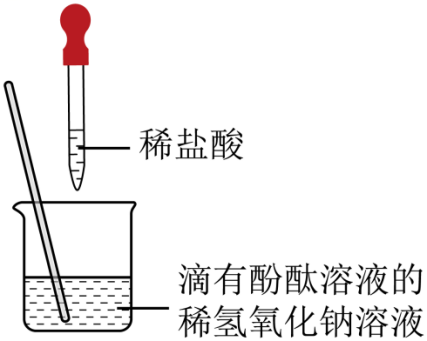
A.加入稀盐酸前溶液为无色 B.搅拌可以使反应物接触更充分
C.反应过程中溶液的pH逐渐增大 D.氢氧化钠与盐酸的反应不属于复分解反应
23.(2023·江苏无锡模拟)如图是稀盐酸与稀氢氧化钠溶液反应过程中溶液pH的变化曲线。下列说法正确的是
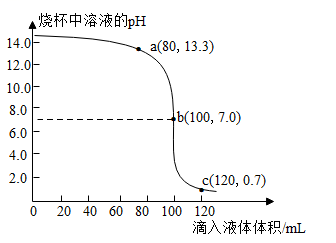
A.a点对应溶液中只有1种溶质
B.实验时将稀氢氧化钠溶液逐滴滴入稀盐酸中
C.b点到c点pH变化的原因是H+和OH-发生反应
D.a点时,参加反应的HCl与NaOH的质量比为36.5:40
24.(2023·福建模拟)为探究稀盐酸和氢氧化钠溶液反应过程中溶液的pH及温度随时间的变化关系,小王按图甲连接好实验装置,往盛有一种溶液的烧杯中滴入另一种初始温度相同的溶液,同时用玻璃棒搅拌。图乙是数字采集器和计算机实时显示的数据曲线,下列说法错误的是
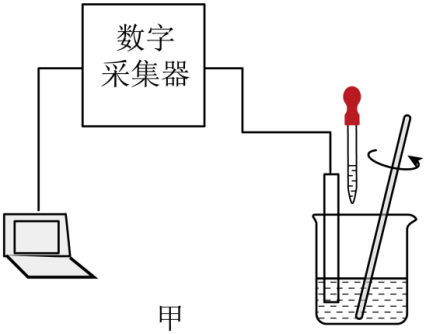
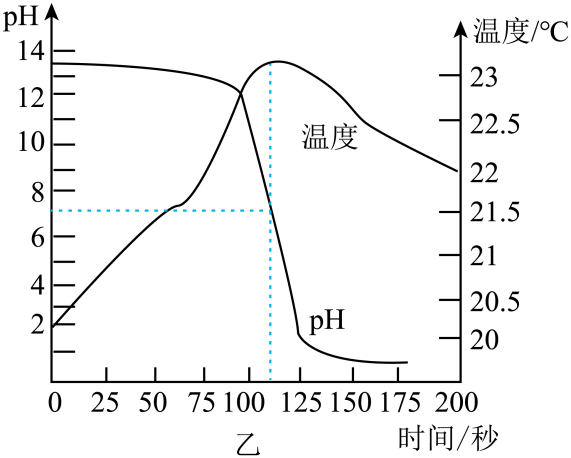
A.实验开始时,烧杯中盛有的试剂是氢氧化钠溶液
B.0~100秒时,温度上升是因为该反应放热
C.100秒时,溶液中Na+和Cl-的个数比是1∶1
D.150秒时,向溶液中放入打磨后的镁条,无明显现象
25.(2023·广东肇庆二模)电导率是衡量溶液导电能力大小的物理量。相同条件下,离子浓度越大,电导率越大。将氢氧化钠溶液不断滴入稀盐酸中,测得滴加过程中的电导率如图所示。下列分析错误的是
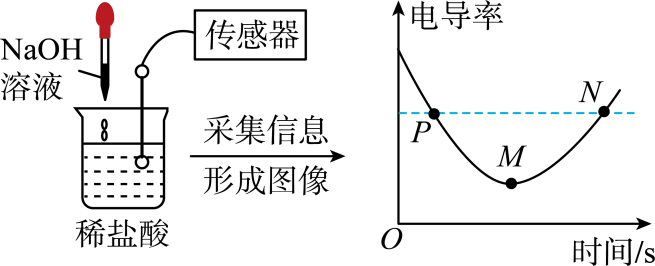
A.该化学反应的实质可表示为<Object: word/embeddings/oleObject25.bin>
B.P点时,溶液中的离子有Na+、Cl-、H+
C.M点时,NaOH溶液与稀盐酸恰好完全反应,但电导率不为零
D.N点溶液中的离子浓度大于P点溶液中的离子浓度
26.(2023·山东泰安二模)稀硫酸与氢氧化钠溶液反应时,测得溶液pH的变化如图所示,溶液温度的变化如图所示。下列说法正确的是
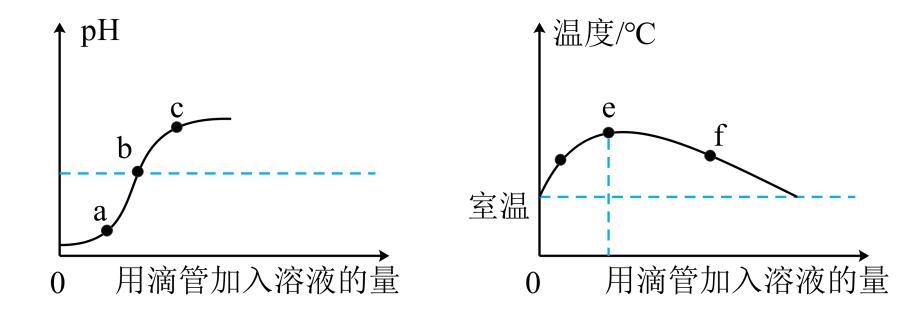
A.该实验是将稀硫酸逐滴滴入一定量的氢氧化钠溶液中
B.图中温度曲线从室温上升到e点,说明该反应是放热反应
C.d点所示溶液pH>7,能使无色酚酞试液变成红色
D.a到c段过程中不断有硫酸钠生成
27.(2023·河南南阳二模)向滴有酚酞的NaOH溶液中逐滴滴入稀盐酸。溶液pH随加入稀盐酸质量的变化曲线如图所示。下列有关说法不正确的是
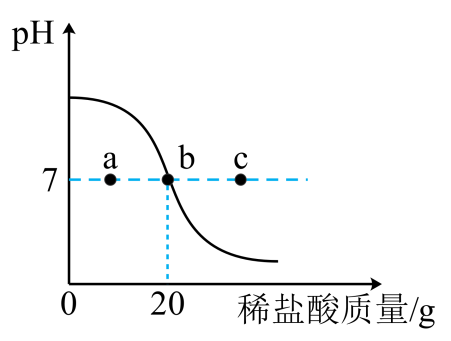
A.反应过程中生成的氯化钠不断增加
B.溶液显无色,说明酸、碱恰好完全反应
C.溶液pH的变化证明了NaOH与稀盐酸发生了反应
D.若稀盐酸换为稀硫酸,则曲线经过c点
28.(2023·山东济南二模)下图为硫酸与氢氧化钡溶液反应时,利用数字化实验测得混合溶液中pH的变化情况。下列说法中不正确的是

A.该操作是将硫酸滴入氢氧化钡溶液中
B.a点所示溶液中含有的溶质是Ba(OH)2
C.b点表示硫酸与氢氧化钡溶液恰好完全反应
D.向c点所在溶液中滴加酚酞,溶液呈红色
参考答案
1.D
【解析】A、根据图像可以看出,开始时溶液的pH大于7,溶液呈碱性,故该实验是将稀硫酸逐滴滴入氢氧化钡溶液中。A正确;
B、由a点到b点发生中和反应,故溶液的温度升高。B正确;
C、a点时硫酸和氢氧化钡没有完全反应,氢氧化钡有剩余;b点时硫酸与氢氧化钡恰好完全反应;c、d点时硫酸与氢氧化钡完全反应,生成硫酸钡沉淀,硫酸有剩余。所以c点时,溶液中只有硫酸一种溶质。C正确;
D、根据<Object: word/embeddings/oleObject26.bin>、<Object: word/embeddings/oleObject27.bin>可知消耗等质量的氢氧化钡需盐酸质量少于硫酸,即b点左移。D错误。
综上所述:选择D。
2.C
【解析】A、由图乙可知,一开始pH>7,随着反应的进行,pH逐渐减小至小于7,故实验开始时,烧杯中盛有的试剂是氢氧化钠溶液,不符合题意;
B、0~100秒时,温度逐渐升高,是因为氢氧化钠和稀盐酸反应放热,不符合题意;
C、100秒时,pH=7,此时氢氧化钠和稀盐酸恰好完全反应生成氯化钠和水,故此时溶液中溶质为氯化钠,溶液中含有的微粒是:Na+、Cl-、H2O,符合题意;
D、150秒时,pH<7,此时稀盐酸过量,向溶液中加入氧化铁粉末,氧化铁和稀盐酸反应生成氯化铁和水,故溶液会变黄色,不符合题意。
故选C。
3.D
【解析】A、硫酸和氢氧化钡反应生成硫酸钡白色沉淀和水,所以试验过程中有白色沉淀生成,故A错误;
B、当稀硫酸和氢氧化钡恰好完全反应时,此时水槽中只有水和硫酸钡沉淀,水槽中液体不导电,所以此时灯泡会熄灭,但是液体中含有水分子,故B错误;
C、稀硫酸和氢氧化钡反应的过程中,硫酸根离子、钡离子、氢氧根离子和氢离子浓度都在变化,故C错误;
D、当用稀盐酸替换稀硫酸时,盐酸和氢氧化钡反应生成氯化钡和水,溶液中始终存在可自由移动的带电粒子钡离子和氯离子,所以溶液会一直导电,实验过程中不会出现灯泡熄灭的情况,所以变化情况不同于滴加稀硫酸的实验,故D正确;
故选D。
4.A
【解析】A、中和反应的实质是氢离子和氢氧根离子结合生成水分子,符合题意;
B、由图可知,一开始pH<7,随着反应的进行,pH逐渐增大至大于7,故该实验是将碱滴入酸溶液中,不符合题意;
C、反应后溶液的质量=酸的质量+滴入碱的质量,n点滴入碱溶液的质量大于m点滴入碱溶液的质量,故n点溶液的质量大于m点溶液的质量,不符合题意;
D、p点溶液pH>7,显碱性,滴加酚酞溶液,溶液变红,不符合题意。
故选A。
5.A
【解析】A、因为a点稀盐酸和氢氧化钠发生反应生成氯化钠,并且pH大于7还有剩余的氢氧化钠,故A正确;
B、c点的溶液呈酸性,不会使无色酚酞溶液变色,故B错误;
C、由氢氧化钠溶液与稀盐酸反应的微观示意图,反应的实质是氢离子和氢氧根离子结合生成水分子,故C错误。
D、由氢氧化钠溶液与稀盐酸反应的微观示意图可知,反应前后氯离子没有改变,故D错误。
故选:A
6.B
【解析】A、久置的氢氧化钠会发生变质,生成碳酸钠,碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,a~b段比b~c段溶液质量增加较慢,说明有碳酸钠参加反应,故a~b段可观察到有气泡产生,正确;
B、向稀硫酸溶液中滴加久置氢氧化钠,碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,氢氧化钠和硫酸反应产生硫酸钠和水,由图知,a点处硫酸过量,故溶液中的溶质有硫酸和硫酸钠两种,故溶液中溶质有2种,错误;
C、由图知,a点硫酸过量,显酸性,pH小于7; c点滴加氢氧化钠量最多,与稀硫酸完全反应,溶液趋碱性,pH大于7;b点介于a、c之间,pH接近7;故a、b、c三点处溶液的pH依次增大,正确;
D、由图可知,a~b段比b~c段溶液质量增加较慢,说明有碳酸钠参加反应,a~b段可观察到有气泡产生,反应是变质的氢氧化钠溶液加入硫酸中,b点硫酸反应完全,故氢氧化钠可以是完全变质,正确。
故选B。
7.D
【解析】A、磁力搅拌器的作用是搅拌,加快反应速率,故A说法错误;
B、图像中的温度变化不能确定是哪种溶液滴向另一种溶液,故B说法错误;
C、由图可知,随着溶液的滴入,温度逐渐升高,可知稀盐酸和氢氧化钠反应是放热反应,温度最高时,稀盐酸与氢氧化钠溶液恰好完全反应,90s是在温度最高之后,故此时稀盐酸或氢氧化钠过量,此时溶液中的溶质不只有氯化钠,故C说法错误;
D、若向稀盐酸中滴加氢氧化钠溶液时,溶液的pH从小于7逐渐的增大到7,最后氢氧化钠过量后大于7,若向氢氧化钠溶液中滴加稀盐酸时,溶液的pH从大于7逐渐的减小到7,最后稀盐酸过量后小于7,用pH传感器代替温度传感器也能探究稀盐酸与氢氧化钠是否发生化学反应,即也可以达到实验目的,故D说法正确;
故选:D。
8.D
【解析】A、由分析可知:所用盐酸的浓度由大到小的顺序为a>b>c,故A错误,不符合题意;
B、在a曲线所示的实验中,图中A点所示溶液的pH大于7,说明氢氧化钠有剩余,则其中所含的溶质有NaCl和NaOH,故B错误,不符合题意;
C、在a、b、c三种曲线所示的实验中,所用盐酸的浓度由大到小的顺序为a>b>c,故反应需要时间依次增大,溶液红色最先褪去的是a(浓度最大),故C错误,不符合题意;
D、由图可知:20min时三种溶液的pH:a<b<c,故溶液的酸性由强到弱的顺序是 a>b>c,故D正确,符合题意。
故选:D。
9.A
【解析】A、浓硫酸沾到皮肤上,应先用大量的水冲洗,然后再涂上3%—5%的碳酸氢钠溶液,而烧碱是氢氧化钠的俗称,氢氧化钠具有腐蚀性,不能涂抹氢氧化钠溶液,故A选项符合题意;
B、氢氧化钠能和油污反应,因此氢氧化钠可用作炉具清洁剂,用于除去油污,故B选项不符合题意;
C、蚊虫叮咬后会分泌蚁酸,从而会感觉痛痒,肥皂水显碱性,涂抹肥皂水能够中和蚁酸,从而消除痛痒,故C选项不符合题意;
D、熟石灰是氢氧化钙的俗称,氢氧化钙是碱,能和酸性物质发生反应,可用于改良酸性土壤,故D选项不符合题意。
故选A。
10.B
【解析】A、由图可知,b点时溶液pH=7,表示酸碱恰好反应,又由于反应过程中,温度先增大后减小,则说明中和反应为放热反应,且e点温度最高,表示此时恰好反应,该选项说法正确;
B、刚开始溶液pH<7,最终pH>7,则该实验是将氢氧化钠逐滴滴入稀硫酸中,该选项说法错误;
C、图中温度升高,表示该反应放热,该选项说法正确;
D、由于滴加的为氢氧化钠,则说明f点所示溶液pH>7,能使无色酚酞试液变成红色,该选项说法正确。
故选B。
11.D
【解析】A、根据分析甲表示氢氧化钠的质量,乙表示水的质量,故A正确;
B、根据分析加入Ng稀硫酸时,两者恰好完全反应,故B正确;
C、根据分析加入Ng稀硫酸时,两者恰好完全反应,b点位于N点之后,此时氢氧化钠已经反应完全,加入的硫酸过量,所以溶液中的溶质是生成物硫酸钠和过量的硫酸,则阳离子有Na+和H+,故C正确;
D、根据分析加入Ng稀硫酸时,两者恰好完全反应,a点位于N点之前,此时加入的稀硫酸只反应掉一部分氢氧化钠,所以溶质有未反应完全的氢氧化钠、生成物硫酸钠,共两种溶质,故D错误。
故选D。
12.D
【解析】A.由图可知,<Object: word/embeddings/oleObject28.bin>点所示溶液pH>7,氢氧化钠过量,该点所示溶液中的溶质为盐酸与氢氧化钠反应生成的NaCl和NaOH,故A错误;
B.由图可知,m点所示溶液pH<7,溶液显酸性,n点所示溶液pH=7,溶液显中性,酚酞溶液在酸性和中性溶液中都不变色,故B错误;
C.由图可知,溶液起始pH<7,随反应的进行,溶液pH逐渐增大,恰好反应等于7,随后大于7,所以该图所对应操作是将氢氧化钠溶液滴入盐酸中,故C错误;
D.该反应是盐酸与氢氧化钠反应生成氯化钠和水,属于中和反应,中和反应的本质是溶液中的<Object: word/embeddings/oleObject29.bin>与<Object: word/embeddings/oleObject30.bin>反应生成水,故D正确。
故选:D。
13.D
【解析】A. 由图像可知,加入另一种溶液前,三颈烧瓶中盛放溶液的pH<7,溶液显酸性。所以X 溶液是稀盐酸,此选项错误;
B. 由图像可知,0—40s溶液的pH逐渐增大,是溶液的碱性增强,<Object: word/embeddings/oleObject31.bin>数量不断增加,此选项错误;
C. 由图像可知,60s时溶液的pH>7,溶液显碱性,其中存在的离子有<Object: word/embeddings/oleObject32.bin>、Na+、Cl-,此选项错误;
D. 由图像可知,温度到达M点说明两者反应放热,此选项正确。
故选D。
14.A
【解析】A、氢氧化钠和盐酸反应生成氯化钠和水,本质反应是氢氧根离子和氢离子结合生成水分子,所以滴加过程中,锥形瓶内溶液中 Na+的数目不断增加,故A正确;
B、溶液为红色说明氢氧化钠过量,则溶液显碱性,pH>7,故B错误;
C、中和反应放热,反应过程中温度不断升高,等盐酸完全反应后,再滴加氢氧化钠溶液,温度不再升高,故C错误;
D、滴加结束后,氢氧化钠过量,所以取少量溶液蒸干,所得白色固体是NaCl、NaOH,故D错误。
故选A。
15.B
【解析】①向一定量<Object: word/embeddings/oleObject33.bin>和<Object: word/embeddings/oleObject34.bin>的混合溶液中,逐滴加入NaOH溶液至过量,最终溶液中有氢氧化钠存在,溶液显碱性,其pH>7,错误;
②硫酸根离子和氢氧化钠不反应,故体系中硫酸根离子数量保持不变,故溶液中硫元素质量保持不变,正确;
③向一定量<Object: word/embeddings/oleObject35.bin>和<Object: word/embeddings/oleObject36.bin>的混合溶液中,逐滴加入NaOH溶液至过量,氢氧化钠首先与硫酸反应生成硫酸钠和水,待硫酸完全消耗后,氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,直至溶液中硫酸铜被完全消耗,沉淀质量保持不变,故需要滴加一部分氢氧化钠溶液后才生成沉淀,正确;
④由③解析知,反应一开始就生成硫酸钠,故一滴加氢氧化钠溶液就会生成硫酸钠,错误;
故正确的有②③,故选B。
16.C
【解析】A、M点电导率最小,则说明此时恰好反应,则P点时表示加入的氢氧化钠还未将盐酸完全反应,则P点的溶质为氯化钠和氯化氢,溶液中的阳离子为钠离子和氢离子,故选项说法正确;
B、M点时溶液的电导率最小,即溶液中离子浓度最小,即NaOH溶液与稀盐酸恰好完全反应,M到N时,氢氧化钠溶液过量,溶液呈碱性,故选项说法正确;
C、P到M,离子数目没有减少,只是溶液体积增大,离子浓度减小,因此电导率减小,故选项说法错误;
D、N点时溶液的电导率与P点时相同,但是N点时溶液的体积大于P点时溶液的体积,说明N点时溶液中的离子数大于P点,故选项说法正确。
故选C。
17.D
【解析】A、向一定体积4%的<Object: word/embeddings/oleObject37.bin>溶液中逐滴加入稀盐酸,溶液的pH随着滴加的盐酸体积的增大而减小。故A正确;
B、酸碱中和反应是放热反应,故溶液的温度随着滴入盐酸体积的增大而增大,当<Object: word/embeddings/oleObject38.bin>被消耗完时,加入盐酸,溶液的温度下降。故B正确:
C、溶液中<Object: word/embeddings/oleObject39.bin>的质量分数先随着加入盐酸体积的增大而增大,然后当二者完全中和后,溶液中氯化钠的质量分数随着盐酸的加入而减小。故C正确;
D、溶液中的<Object: word/embeddings/oleObject40.bin>的质量在二者完全中和减小至0,后质量一直为0。故D错误。
故选D。
18.C
【解析】A、由图示可知,a点时,烧杯中溶液的pH>7,正确。
B、b点时溶液的pH=7,溶液显中性,溶液中H+和OH-恰好完全反应,正确。
C、c点时溶液的pH<7,显酸性,酸性溶液不能使酚酞试液变红,c点时,烧杯中的溶液显无色,错误。
D、氢氧化钠和稀盐酸反应生成氯化钠和水,在滴入稀盐酸的过程中溶液里Na+数目不变,正确。
故选:C。
19.C
【解析】A、碳酸钠与稀盐酸的反应的反应物不是酸和碱,生成物不是盐和水,不属于中和反应 ,错误;
B、生成盐和水的反应不一定是中和反应 ,例如氧化铜与水反应,虽生成盐和水,但反应物不是酸和碱,不属于中和反应 ,错误;
C、中和反应的微观实质是酸溶液中的H+和碱溶液中的OH-反应生成H2O ,正确;
D、有些中和反应都有明显现象,例如氢氧化钡与硫酸反应生成硫酸钡沉淀和水,错误。
故选C。
20.B
【解析】A、用盐酸除铁锈,利用的铁锈的主要成分氧化铁与稀盐酸反应生成氯化铁和水,不是酸与碱的反应,不属于中和反应,不是利用了中和反应原理,故选项错误;
B、氨水处理废水中的硫酸,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项正确;
C、碳酸钙和胃液中的盐酸反应,生成可溶性的氯化钙,从而被人体吸收,可用作补钙剂,不是酸与碱的反应,不属于中和反应,故选项错误;
D、服用含有氧化镁的药物治疗胃酸过多,该反应是酸与金属氧化物反应生成盐和水的反应,不属于中和反应,故选项错误。
故选B。
21.A
【解析】A、由图可知,a点pH<7,此时硫酸还未完全反应,氢氧化钾和硫酸反应生成硫酸钾和水,故此时溶质是:硫酸钾和硫酸,符合题意;
B、c点pH>7,显碱性,能使无色酚酞试液变红,不符合题意;
C、由分析可知,该实验是将氢氧化钾溶液滴入稀硫酸中,不符合题意;
D、b点pH=7,此时氢氧化钾和稀硫酸恰好完全反应,此时溶液中的溶质是硫酸钾,溶液中的微粒是钠离子和硫酸根离子,不符合题意。
故选A。
22.B
【解析】A、氢氧化钠是碱,其溶液呈碱性,能使酚酞溶液变红,则加入稀盐酸前溶液为红色,选项错误;
B、搅拌可以使反应物接触更充分,反应更充分,选项正确;
C、氢氧化钠溶液呈碱性,滴加稀盐酸,和稀盐酸生成氯化钠和水,氯化钠溶液呈中性,酸过量,溶液呈酸性,反应过程中溶液的pH逐渐减小,选项错误;
D、氢氧化钠与盐酸生成氯化钠和水,反应是两种化合物互相交换成分,生成另外两种化合物的反应,属于复分解反应,选项错误。
故选B。
23.D
【解析】A、a点对应溶液呈碱性,溶液中含有氯化钠和未反应完的氢氧化钠,错误;
B、实验过程中溶液的pH逐渐减小,说明是将稀盐酸逐滴滴入稀氢氧化钠溶液中,错误;
C、b点到c点pH由7变化为小于7,反应已经结束,变化的原因是酸过量,错误;
D、a点时,氢氧化钠和稀盐酸反应生成氯化钠和水,根据化学反应方程式可知,每36.5份质量的氯化氢会和40份质量的氢氧化钠反应,参加反应的HCl与NaOH的质量比为36.5:40,正确。
故选:D。
24.D
【解析】A、由图乙可知,一开始pH>7,随着反应的进行,pH逐渐减小至小于7,故实验开始时,烧杯中盛有的试剂是氢氧化钠溶液,不符合题意;
B、0~100秒时,温度逐渐升高,是因为氢氧化钠和稀盐酸反应放热,不符合题意;
C、100秒时,pH=7,此时氢氧化钠和稀盐酸恰好完全反应生成氯化钠和水,故此时溶液中钠离子和氯离子的个数比是1:1,不符合题意;
D、150秒时,pH<7,此时稀盐酸过量,向溶液中放入打磨后的镁条,镁和稀盐酸反应生成氯化镁和氢气,产生大量气泡,符合题意。
故选D。
25.D
【解析】A、该化学反应是氢氧化钠与盐酸的中和反应,所以该化学反应的实质可表示为H++OH−=H2O。A正确;
B、P点时,溶液中的溶质是生成的氯化钠和未反应的盐酸,所以P点时,溶液中的离子有Na+、Cl-、H+。B正确;
C、M点时电导率最低,NaOH溶液与稀盐酸恰好完全反应,溶液中的溶质是生成的氯化钠,溶液中的离子有Na+、Cl-。所以电导率不为零。C正确;
D.据图可知,由于N点和P点电导率相等,所以N点溶液中的离子浓度等于P点溶液中的离子浓度。D错误。
综上所述:选择D。
26.B
【解析】A、图像中起始溶液pH小于7,呈酸性,说明该反应是将氢氧化钠溶液逐滴滴入稀硫酸中,故选项说法不正确;
B、图中温度曲线从室温上升到e点,温度升高,说明该反应是放热反应,故选项说法正确;
C、d点时溶液温度没有达到最高,说明稀硫酸没有反应完,pH<7,溶液呈酸性,所以该点的溶液不能使无色酚酞变红,故选项说法不正确;
D、b点的溶液pH=7,呈中性,即b点时酸与碱恰好完全反应,因此a到b段过程中不断有硫酸钠生成,而b点后没有发生化学反应,没有硫酸钠生成,故选项说法不正确。
故选B。
27.B
【解析】A、向滴有酚酞的NaOH溶液中逐滴滴入稀盐酸,稀盐酸与氢氧化钠反应生成氯化钠和水,所以说反应过程中生成的氯化钠不断增加,故A说法正确;
B、氢氧化钠显碱性,能够使无色酚酞变红,滴有酚酞的氢氧化钠溶液显红色,随着稀盐酸的滴入,稀盐酸与氢氧化钠反应生成氯化钠和水,当溶液由红色恰好变为无色时,说明酸与碱恰好完全反应,当盐酸过量时,溶液也是无色的,故B说法错误;
C、氢氧化钠显碱性,pH>7,随着稀盐酸的滴入,溶液的pH逐渐减小到7,直至小于7,证明氢氧化钠与稀盐酸发生了反应,故C说法正确;
D、氢氧化钠与盐酸反应生成氯化钠和水,该反应方程式为<Object: word/embeddings/oleObject41.bin>,36.5份质量的盐酸与40份质量的氢氧化钠恰好完全反应,此时溶液 的pH=7,氢氧化钠与硫酸反应生成硫酸钠和水,该反应方程式为<Object: word/embeddings/oleObject42.bin>,98份质量的硫酸与80份质量的氢氧化钠恰好完全反应,此时溶液的pH=7,等质量的氢氧化钠完全反应时,消耗稀硫酸较多,所以若稀盐酸换为稀硫酸,则曲线经过c点,故D说法正确;
故选B。
28.D
【解析】A、由图可知,起点处溶液的pH大于7,溶液呈碱性,加入某种溶液后,溶液的pH逐渐减小,最终溶液的pH小于7,呈酸性,则该操作是将硫酸滴入氢氧化钡溶液中,选项正确;
B、硫酸与氢氧化钡反应生成硫酸钡沉淀和水,由图可知,a处溶液的pH大于7,呈碱性,则溶液中的溶质是未反应的氢氧化钡,选项正确;
C.由图可知,b处溶液的pH等于7,溶液呈中性,则b点表示硫酸与氢氧化钡溶液恰好完全反应,选项正确;
D、由图可知,c点溶液的pH小于7,溶液呈酸性,则向c点所在溶液中滴加酚酞,酚酞不变色,溶液呈无色,选项错误,故选D。
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图