讲授新课
| 教师利用多媒体设备向学生投影出下面
新课讲解:比较氯、溴和碘的非金属性强弱
教师:(1)在点滴板的3个孔穴中分别滴入3滴NaBr溶液、NaI溶液和新制的氯水,然后向NaBr溶液和NaI溶液中各滴入3滴新制的氯水。观察颜色变化,并与氯水的颜色进行比较。写出反应的化学方程式。
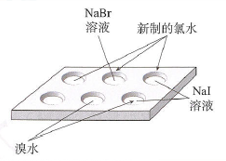
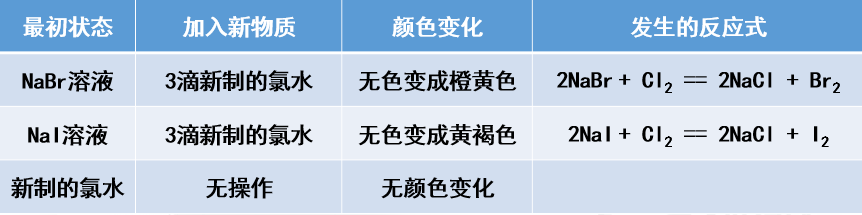
新课讲解:比较氯、溴和碘的非金属性强弱
教师:(2)在点滴板的2个孔穴中分别滴入3滴NaI溶液和溴水,然后向NaI溶液中各滴入3滴溴水。观察颜色变化,并与溴水的颜色进行比较。写出反应的化学方程式。
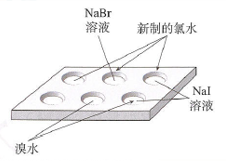

思考讨论:教师:实验中所用的氯水为什么要用新制的?
答案:因为氯水中溶解的氯气部分能够与水反应,生成盐酸和次氯酸,次氯酸不稳定,受光易分解产生氧气,最终氯水变为盐酸。
思维启迪:氯、溴和碘的非金属性强弱
现象:Cl2能从NaBr中置换出Br2,从NaI中置换出I2
结论:因此Cl2的非金属性强于Br2,也强于I2
现象:Br2能从NaI中置换出I2
结论:因此Br2的非金属性强于I2
最终结论:他们的非金属性由强到弱的排序为:Cl2>Br2>I2
新课讲解:比较钠、镁和铝的金属性强弱
教师:①回忆钠与水反应的实验,写出实验现象和化学方程式。
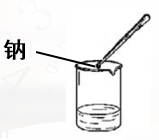

新课讲解:比较钠、镁和铝的金属性强弱
②回忆镁与冷水、热水的反应,观察并记录实验现象。
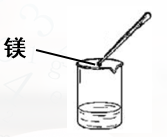

思考讨论:教师:实验中为什么要将镁条用砂纸打磨至光亮?
答案:因为Mg是强氧化剂,放在空气中有MgO生成,MgO是氧化物。氧化反应的速度比较慢,所以,把镁条打磨光是为了让单质镁能够以最大的面积接触空气中的氧气。
新课讲解:比较钠、镁和铝的金属性强弱
教师:(2)通过MgCl2、AlCl3与NaOH的反应,比较Mg(OH)2、Al(OH)3的碱性强弱。
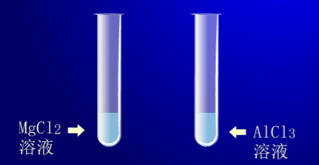

思维启迪:钠、镁和铝的金属性强弱
现象:Na能和冷水反应,Mg不能和冷水反应,只能和热水反应
结论:因此Na的金属性强于Mg
现象:过量氢氧化钠溶液会使氢氧化铝沉淀溶化,氢氧化镁则不受影响。
结论:因此Mg的金属性强于Al
最终结论:他们的金属性由强到弱的排序为:Na>Mg>Al
思考讨论:教师:通过以前的知识和上述实验,你能得出哪些结论?
课堂达标
1.填写下列空格
氯、溴和碘的非金属性强弱__________
钠、镁和铝的金属性强弱____________
氢氧化镁和氢氧化铝碱性强弱_______
解析:氯、溴和碘非金属性由强到弱的排序为:Cl2>Br2>I2,钠、镁和铝的金属性由强到弱的排序为:Na>Mg>Al,氢氧化镁和氢氧化铝碱性由强到弱的排序为:Mg(OH)2>Al(OH)3。
2.下图表示碱金属的某些性质与核电荷数的变化关系,下列各性质中不符合图示关系的是( )
A.还原性
B.与水反应的剧烈程度
C.熔点
D.原子半径
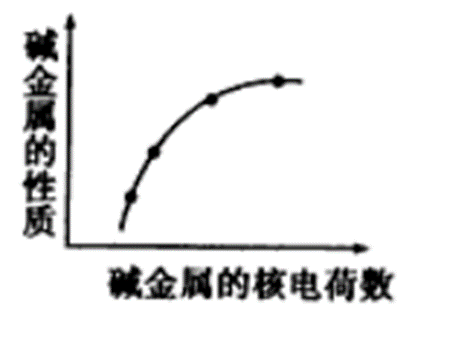
解析:选项A中,碱金属元素中,随着碱金属的核电核数的增大,元素的金属性逐渐增强,单质的还原性逐渐增强,故A的说法正确;选项B中,碱金属元素中,随着碱金属的核电核数的增大,元素的金属性逐渐增强,与水反应的剧烈程度逐渐增大,故B的说法正确;选项C中,碱金属元素中,随着碱金属的核电核数的增大,金属晶体的金属键作用力减弱,熔点逐渐降低,故C的说法错误;选项D中,碱金属元素中,随着碱金属的核电核数的增大,核外电子层数逐渐增多,电子层数越多,半径越大,故D的说法正确。因此选C
3.金属钾和金属钠的性质相似,下列说法中能最好地解释这个事实的是( )
A.都是金属元素
B.原子半径相差不大
C.最外层电子数相同
D.最高化合价相同
解析:物质的性质是由结构决定的,钾和钠的性质相似,则说明钾和钠的结构相似即最外层电子数相同,均有1个电子。选项C的描述是正确的,因此选C。
4.运用元素周期律分析下面的推断,其中推断错误的是( )
A.氢氧化铍[Be(OH)2]的碱性比氢氧化镁弱
B.砹(At)为有色固体,HAt不稳定
C.硫酸锶(SrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)是无色、有毒,比H2S稳定的气体
解析:选项A中,Be和Mg同主族,Mg的核电荷数大于Be,金属性比Be强,因此碱性比较:Be(OH)2<Mg(OH)2,A项正确;选项B中,卤族元素的单质从上到下,颜色加深,氢化物越来越不稳定,B项正确;选项C中,Sr和Ba同主族,故SrSO4也难溶于水,C项正确;选项D中,Se的非金属性不如S强,故H2Se不如H2S稳定,D项错误。因此选D。
| 认真观察实验现象,并填写表格。
认真观察实验现象,并填写表格。
老师和同学一起讨论,思考问题。
记录笔记,认真倾听。
认真观察实验现象,并填写表格。
认真观察实验现象,并填写表格。
老师和同学一起讨论,思考问题。
认真观察实验现象,并填写表格。
记录笔记,认真倾听。
老师和同学一起讨论,思考问题。
学生自行思考,完成课堂练习。
| 通过实际操作,帮助同学理解和记忆知识点。
通过实际操作,帮助同学理解和记忆知识点。
通过讨论,帮助同学对知识点的掌握。
通过书写和口述帮助学生对知识点进行记忆。
通过实际操作,帮助同学理解和记忆知识点。
通过实际操作,帮助同学理解和记忆知识点。
通过讨论,帮助同学对知识点的掌握。
通过实际操作,帮助同学理解和记忆知识点。
通过书写和口述帮助学生对知识点进行记忆。
通过讨论,加深对知识点的印象。
通过对习题的解答,加深对知识点的巩固。
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图