|
|
影响粒子半径大小的因素有:
①电子层数的多少;
②原子核对核外电子的吸引力的大小;
③核外电子的多少。
(1)同周期、同主族原子半径的比较
①同一周期,从左到右,核电荷数依次增大,
原子半径依次减小。如r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl)。
②同一主族,自上而下,电子层数依次增多,
原子半径依次增大。如r(Li)<r(Na)<r(K)<r(Rb)<r(Cs)。
(2)任意简单粒子半径的比较
①先看电子层数,层多径大,如r(Cl)>r(O)。
②电子层数相同时看核电荷数,荷少径大,
如r(F-)>r(Na+)。
③电子层数、核电荷数都相同时看电子数,
电子数多的半径大,如r(Cl-)>r(Cl)、r(Fe2+)>r(Fe3+)。
1.下列各组微粒半径大小的比较中,错误的是()
A.K>Na>Li B.Mg2+>Na+>F﹣
C.Na+>Mg2+>Al3+ D.Cl﹣>F﹣>F
【答案】B
详解:A.同主族自上而下原子半径增大,
故原子半径K>Na>Li,A正确;
B.核外电子排布相同,核电荷数越大离子半径越小,
故离子半径F->Na+>Mg2+,B错误;
C.核外电子排布相同,核电荷数越大离子半径越小,
故离子半径Na+>Mg2+>Al3+,C正确;
D.最外层电子数相同,电子层越多离子半径越大,
阴离子半径大于相应的原子半径,故半径Cl->F->F,D正确;
(1)主族元素的最高化合价=族序数(O、F除外)。
(2)非金属元素最低负价=8-原子的最外层电子数(H除外)。
2.某同主族(或同周期)元素的主要化合价的变化规律如右图所示,它们可能位于周期表
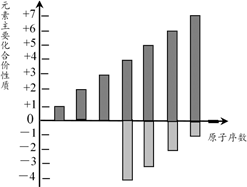
A.ⅠA族 B.ⅡA族
C.第二周期 D.第三周期
【答案】D
【解析】A、若为ⅠA族,化合价均为+1价,选项A错误;B、若为ⅡA族,化合价均为+2价,选项B错误;C、若为第二周期,F元素没有正价,选项C错误;D、若为第三周期,符合最高正价从+1到+7,负价由硅的-4到Cl的-1,选项D正确。答案选D。
(1)预测未知元素的性质
依据:同主族元素性质的递变规律。
如已知卤族元素的性质递变规律,可推知未知元素砹(At)应为有色固体,与氢难化合,HAt不稳定,水溶液呈酸性,AgAt不溶于水等。
3.1.(2019·衡水高一检测)原子序数为114的元素位于第七周期第ⅣA族,称为类铅元素。下面关于它的原子结构和性质的说法正确的是 ( )
A.类铅元素原子的最外层电子数为6
B.其常见价态为+2、+3、+4
C.它的金属性比铅强
D.它的原子半径比铅小
【解析】选C。114号元素位于第ⅣA族,最外层电子数应该是4,A项错;C、Si、Pb的常见正价有+2、+4价,没有+3价,B项错;同主族元素的金属性由上至下逐渐增强,C项正确;该元素的电子层数比Pb多,原子半径比Pb大,D项错
(2)比较元素的性质
依据:元素周期律。
如比较H2SO4和H2SeO4的酸性强弱,因为S、Se同主族,自上至下,元素的非金属性减弱,最高价氧化物对应的水化物酸性减弱,故酸性:H2SO4>H2SeO4。
3.2(2019·临沂高一检测)门捷列夫对化学这一学科发展的最大贡献在于发现了化学元素周期律。下列事实不能用元素周期律解释的只有 ( )
A.碱性:KOH>Ca(OH)2>Mg(OH)2
B.稳定性:H2O>H2S>H2Se
C.挥发性:HNO3>H3PO4>H2SO4
D.原子半径 >S>Cl >S>Cl
【解析】选C。元素的金属性越强,其原子失电子能力越强,其最高价氧化物对应的水化物碱性越强,金属性K>Ca>Mg,则碱性:KOH>Ca(OH)2>Mg(OH)2,A可以;元素的非金属性越强,其对应的气态氢化物越稳定,同主族元素非金属性O>S>Se,则稳定性:H2O>H2S>H2Se,B可以;挥发性与物质的结构无关,C不可以;同周期元素从左到右原子半径逐渐减小,D可以。
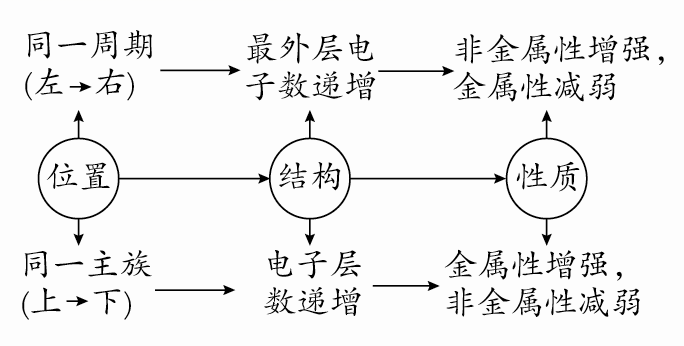
4.(2019·济南高一检测)短周期主族元素X、Y、A、B、C在元素周期表的位置如图所示,A是非金属性最强的元素,则下列说法不正确的是 ( )
A.原子半径由小到大的顺序为A<B<C<Y
B.A、B的氢化物的稳定性强弱顺序为HA<HB
C.X、Y最高价氧化物对应的水化物的酸性由弱到强的顺序为H2YO3<H2XO3
D.B、C简单离子的还原性由弱到强的顺序为B-<C2-
【解析】选B。A是非金属性最强的元素即为氟元素,故X、Y、B、C分别为C、Si、Cl、S。B、C、Y在同一周期,随原子序数的递增,原子半径逐渐减小,故B<C<Y,A在上一周期,电子层数少,原子半径最小,故原子半径由小到大的顺序为A<B<C<Y,A项正确;F、Cl对应氢化物的稳定性HF>HCl,B项错误;X、Y位于同一主族,随原子序数的增大,非金属性逐渐减弱,最高价氧化物对应的水化物的酸性逐渐减弱,故酸性由弱到强的顺序为H2YO3<H2XO3,C项正确;B、C位于同一周期,简单离子的电子层排布相同,但是核内质子数越多,离子半径越小,还原性越弱,故还原性由弱到强的顺序为B-<C2-,D项正确。
元素“位构性”中的注意点(1)注意原子核外最外层有1个或2个电子,既可能是第ⅠA族、第ⅡA族元素,也可能是副族、第Ⅷ族或0族元素。
(2)铝及其氧化物、氢氧化物都具有两性,但锗等金属元素与非金属元素分界线附近的元素的单质及其相应化合物不具有两性。
(3)非金属性最强的元素是F,但最高价氧化物对应水化物的酸性最强的元素是Cl(HClO4)。
(4)一般来说,元素的性质越活泼,其单质的性质也就越活泼,但N与P却相反,N的非金属性强于P,但N2比红磷、白磷更稳定。
由于新教材对铝三角的转化和计算淡化,所以这里只是整理一些基础内容,还是看看价类二维图。

5、铝
(1)铝与酸或碱反应中的比例关系
| 方程式
| 比例关系
| 与酸
反应
| 2Al+6HCl===2AlCl3+3H2↑
| 2Al~6HCl~2AlCl3~3H2
| 与碱
反应
| 2Al+2NaOH+2H2O===2NaAlO2+3H2↑
| 2Al~2NaOH~2NaAlO2~3H2
|
(2)铝与酸、碱反应的规律分析(基础差一点的可以不看)
(1)等质量的铝与足量的盐酸、氢氧化钠溶液分别反应:
①生成H2的物质的量之比为1∶1。
②消耗H+、OH-的物质的量之比为n(H+)∶n(OH-)=3∶1。
(2)足量的铝分别与等物质的量的HCl和NaOH反应:
①生成H2的物质的量之比为1∶3。
②消耗Al的物质的量之比为1∶3。
(3)一定量的铝分别与一定量的盐酸、氢氧化钠溶液反应:
5.某同学在实验室利用氢氧化钠、盐酸分离铁粉和铝粉混合物,物质转化关系如图所示:
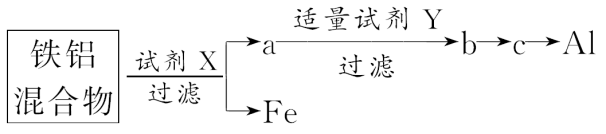
下列说法不正确的是( )
A.X为NaOH溶液,Y为盐酸
C.b→c→Al的反应条件分别为:加热、电解
D.a、b、c既能与酸又能与碱反应
6、含铝的化合物
1.氧化铝
2.氢氧化铝
氢氧化铝是两性氢氧化物,其电离方程式:
碱式电离:Al(OH)3Al3++3OH-;
3.Al2O3与Al(OH)3的比较
化合物
| 氧化铝(Al2O3)
| 氢氧化铝[Al(OH)3]
| 物理性质
| 白色固体,熔点高
| 白色胶状物质,难溶于水
| 化学性质
| 与酸反应
| Al2O3+6H+===2 Al3++3H2O
| Al(OH)3+3H+=== Al3++3H2O
| | 与碱反应
| | | | 加热
| —
| | 制备方法
| | | 主要用途
| 作耐火材料、冶炼铝的原料
| 制药、净水
|
6.(2019·静海一中月考)下列各组物质,不能按a―→b―→c(“―→”表示反应一步完成)关系转化的是()
选项
| a
| b
| c
| A
| Al2O3
| NaAlO2
| Al(OH)3
| B
| AlCl3
| Al(OH)3
| NaAlO2
| C
| Al
| Al(OH)3
| Al2O3
| D
| MgCl2
| Mg(OH)2
| MgO
|
解析:选CAl2O3溶于NaOH溶液生成NaAlO2,NaAlO2溶液中通入CO2生成Al(OH)3,故A正确;AlCl3与氨水反应生成Al(OH)3,Al(OH)3溶于NaOH溶液生成NaAlO2,故B正确;铝不能直接生成Al(OH)3,故C错误;MgCl2与NaOH溶液反应生成Mg(OH)2,Mg(OH)2加热分解生成MgO,故D正确。
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图