|
|
第五章 化工生产中的重要非金属元素
第2节 氮及其化合物
第3课时 硝酸和酸雨及防治

本节是人教版第五章第二节氮及其化合物的内容。本节内容主要包括:氮及氮的固定、一氧化氮和二氧化氮、氨和铵盐、硝酸、酸雨及其防治。教材首先根据氮的原子结构知识,应用前一节掌握的研究非金属单质性质的基本思路预测氮的化学性质,渗透条件对化学反应的影响,引出氮的固定对人类生存的重要意义。之后,根据物质类别研究氮的化合物,包括一氧化氮、二氧化氮、硝酸、氨和铵盐的化学性质。以工业合成氨、工业制硝酸的生产原理为载体,应用氧化还原反应原理,设计含氮化合物的转化,使学生认识到从一种原料转化成多种产品,路径之一是通过氧化还原反应改变主要元素的化合价,提升“变化观念”等学科核心素养。教材设置铵根离子的检验、实验室制取氨的实验活动,让学生根据氨、铵根离子的性质和反应,选择合适的试剂,设计检验或者制取物质的方案,提升其科学探究的能力。最后,教材编入“酸雨及其防治”内容以及“测定雨水的pH”的研究与实践活动,综合运用硫和氮及其化合物的相关知识,寻求证据参与社会性议题的讨论,分析硫酸工业、合成氨工业对社会发展的价值和对环境的影响,有意识地渗透资源合理利用和环境保护的意识。
《普通高中化学课程标准(2017版)》对本节的要求:结合真实情境中的应用实例或通过实验探究,了解氮及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。结合实例认识金属、非金属及其化合物的多样性,了解通过化学反应可以探索物质性质、实现物质转化,认识物质及其转化在自然资源综合利用和环境保护中的重要价值。其情景素材建议为:“雷雨发庄稼”;氮的循环与氮的固定;工业合成氨、工业制硫酸(或硝酸);氮肥的生产与合理使用;氯气、氨气等泄漏的处理;酸雨的成因与防治;汽车尾气的处理。因此内容安排三个课时:第一课时为氮气与氮的固定,一氧化氮和二氧化氮,第二课时为氨和铵盐,第硝酸和酸雨及防治。本节为第二课时的内容:硝酸和酸雨及防治。

【学习目标】
1、能运用氧化还原反应知识理解硝酸的氧化性。
2、认识硝酸在相关反应中体现的性质,了解硝酸的保存方法。
3、了解SO2、NO2对大气质量的影响,特别是酸雨的成因、危害及防治措施。
【核心素养】
1、通过学习硝酸的性质及原子守恒法、电子守恒法的应用,培养学生论据推理与模型认知的化学核心素养。
2、通过酸雨的形成及防治认识化学对人类的作用,培养学生科学态度与社会责任的化学核心素养。


多媒体、硝酸、铜丝、NaOH、具支试管等

【引入】为什么硝酸泄漏会有黄色的气体产生?

【讲解】
一、硝酸
1、物理性质:无色、易挥发、有刺激性气味的液体
2、化学性质:
(1) HNO3的不稳定性
a. 浓硝酸见光或受热时发生反应
b. 贮存:一般将浓硝酸保存在棕色玻璃瓶中,并避光放置于冷暗处
(2) HNO3的强氧化性
① 与Cu反应
【实验探究】
【实验5-8】
如图5-14所示,在橡胶塞侧面挖一个凹槽,并嵌入下端卷成螺旋状的铜丝。向两支具支试管中分别加入2mL浓硝酸和稀硝酸,用橡胶塞塞住试管口,使铜丝与硝酸接触,观察并比较实验现象。向上拉铜丝,终止反应。
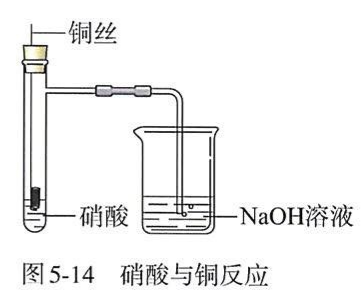
【观看视频】
| 稀硝酸
| 浓硝酸
| 实验
现象
| 反应缓慢,有少量气泡产生,__________,试管口有红棕色气体产生
| 反应剧烈,有__________产生,__________,液面上有________气体产生
| 实验
结论
| 铜与稀硝酸常温下缓慢反应生成_____气体
| 铜与浓硝酸常温下剧烈反应生成_____气体
|
Cu+4HNO3(浓) === Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀) === 3Cu(NO3)2+2NO↑+4H2O
硝酸的浓度不同,与金属反应的产物也不同。
浓硝酸的还原产物为NO2,稀硝酸的还原产物为NO
② 常温下浓硝酸能使Fe、Al发生钝化
③ 与非金属反应
【资料卡片】

劳厄和弗兰克,曾获得1914年和1925年的物理学奖,德国纳粹政府要没收他们的诺贝尔奖牌,他们辗转来到丹麦,请求丹麦同行、1922年物理学奖得主玻尔帮忙保存。1940年,纳粹德国占领丹麦,受人之托的玻尔急得团团转。同在实验室工作的一位匈牙利化学家赫维西(1943年化学奖得主)帮他想了个好主意:将奖牌放入“王水” 中,纯金奖牌便溶解了。玻尔于是将溶液瓶放在实验室架子上,来搜查的纳粹士兵果然没有发现这一秘密。战争结束后,溶液瓶里的黄金被还原后送到斯德哥尔摩,按当年的模子重新铸造,于1949年完璧归赵。
浓硝酸和浓盐酸按体积比为1∶3混合得到的混合物。
能使不溶于硝酸的金属如金、铂等溶解。
【思考与交流】
硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。工业上制硝酸的原理是将氨经过一系列反应得到硝酸,如下图所示:
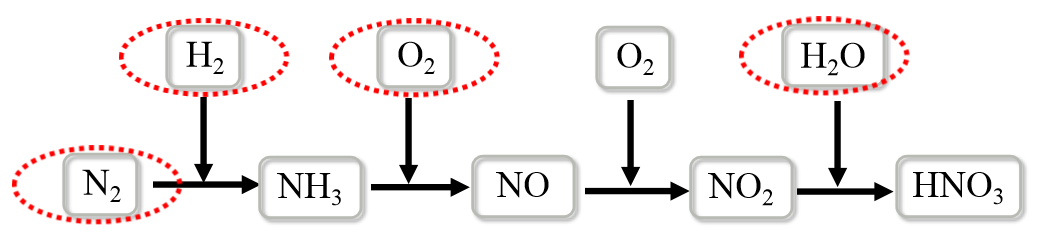
(1) 写出每一步反应的化学方程式。
(2) 请分析上述反应中的物质类别和氮元素化合价的变化情况,以及每一步反应中含氮物质发生的是氧化反应还是还原反应。
写出有关化学方程式:
N2→NH3:。
NH3→NO:。
NO→NO2:。
NO2→HNO3:。
【讲解】
二、酸雨及防治
煤、石油和某些金属矿物中含有硫,在燃烧或冶炼时往往会生成二氧化硫。在机动车发动机中,燃料燃烧产生的高温条件会使空气中的氮气与氧气反应,生成氮氧化物。它们会引起呼吸道疾病,危害人体健康,严重时会使人死亡。


1. 酸雨的形成
酸雨:主要指 pH小于5.6 的雨水,其主要是含有硫酸和硝酸。
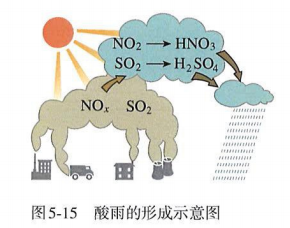
成因:主要是大气中的SO2与NOx溶于水形成的。
硫酸型酸雨:S→SO2→SO3→H2SO4
硝酸型酸雨:NO2→HNO3
2. 酸雨的危害
(1)对人体的直接危害首先是它的刺激性,其次是它会形成硫酸雾和硫酸盐雾,其毒性比SO2大,能浸入人的肺部,引起肺水肿等疾病而使人致死。
(2)引起河流、湖泊的水体酸化,严重影响水生动物生长。
(3)破坏土壤、植被、森林。
(4)腐蚀金属、油漆、皮革、纺织品及建筑材料等。
(5)渗入地下,可引起地下水酸化,酸化后的地下水中铝、铜、锌、镉等对人体有害金属元素的含量会偏高。
3. 酸雨的防治
(1)调整能源结构,积极开发新能源
(2)对煤(其中含硫为0.3%-5%)进行处理,如选洗加工、综合开发、在煤中加入适量的生石灰、对排放的烟进行处理等
(3)种植能够吸收SO2的有关树木(如臭椿、垂柳、柳杉)等
(4)加强工厂废气的回收处理
(5)改进汽车尾气的处理技术,控制尾气排放
【研究与实践】
测定雨水的pH
【研究目的】
酸雨对环境危害巨大,人们已经采取多种措施来防治酸雨。通过以下活动了解测定雨水pH的方法,认识酸雨的危害,激发保护环境的紧迫感。
【研究任务】
(1) 收集资料
a以“酸雨”为关键词进行搜索,了解酸雨的形成原因、基本类型、相关危害及预防和治理措施。|图5-17用出计测量水样的酸度
(2) 测定雨水的pH根据收集的资料,确定测定雨水pH的过程和方法并进行实践,对结果进行分析和讨论。可参考如下过程:
①下雨时用容器直接收集一些雨水作为样品,静置,以蒸馏水或自来水作为参照,观察并比较它们的外观;
②用pH试纸(或pH计)测量雨水和蒸馏水的酸度并记录;
③有条件的话,可连续取样并测定一段时间(如一周)内本地雨水、地表水或自来水的pH,将得到的数据列表或作图,确定你所在地区本时间段内雨水等的平均酸度。
【结果与讨论】
【总结】
【课堂练习】
1. 下述实验中均有红棕色气体产生,对比分析所得结论不正确的是 ( )
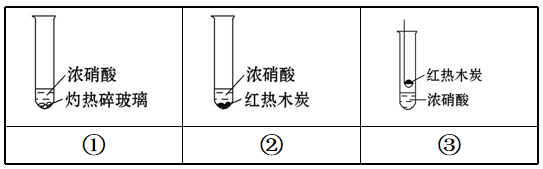
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
2.下列反应中硝酸既能表现出酸性又表现出氧化性的是 ( )
A.使石蕊试液变红
B.与铜反应放出NO气体,生成Cu(NO3)2
C.与Na2CO3反应放出CO2气体,生成NaNO3
D.与S单质混合共热时生成H2SO4和NO2
3. 在标准状况下将1.92 g铜粉投入一定量浓硝酸中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混合气体1.12 L,则混合气体中NO的体积为 ( )
A.112 mL B.1 008 mL C.224 mL D.448 mL
4. 9.7 g Cu和Zn的合金与足量的稀硝酸反应,还原产物只有NO气体,其体积在标准状况下为2.24 L。将溶液稀释为1 L,测得溶液的c(H+)=0.1 mol·L-1,此时溶液中NO3-的浓度为 ( )
A.0.3 mol·L-1 B.0.4 mol·L-1 C.0.2 mol·L-1 D.0.6 mol·L-1
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图