课题
| 第一章 化学反应的热效应
第2节 反应热的计算
|
教学目标
| 知识与技能
| 1、通过探究与实例结合教学,了解盖斯定律的涵义
2、用盖斯定律进行有关反应热的简单计算。
|
| 过程与方法
| 1、通过对盖斯定律的涵义的分析和论证,培养学生分析问题的能力;
2、通过盖斯定律的有关计算,培养学生的计算能力。
|
| 情感态度
与价值观
| 1、通过对盖斯定律的发现过程及其应用的学习,感受化学科学对人类生活和社会发展的贡献。激发参与化学科技活动的热情。
2、通过对天然气的使用效率的研究,加强学生保护能源的意识。
|
教学
重点
| 盖斯定律的涵义和根据盖斯定律进行反应热的计算;
|
教学
难点
| 盖斯定律的应用
|
教 学 设 想
| 教材分析
| 本节内容分两部分,第一部分介绍了盖斯定律;第二部分,利用反应热的概念、盖斯定律和热化学方程式进行有关反应热的计算。本节内容的难点是盖斯定律的应用,为了突破难点,把本节分为两课时完成,第一课时为盖斯定律的理解及简单应用,第二课时为利用盖斯定律等进行化学反应热的综合计算。本节为第一课时。
|
| 学情分析
| 本节课的教学内容是人教版选修4《化学反应原理》第一章第三节的内容。学生在学习了化学反应的能量变化、燃烧热 能源的学习后,继续学习化学反应热的计算,本节介绍了盖斯定律,并从定量的角度让学生加深理解,进一步认识物质发生化学反应伴随的热效应。
|
| 教法设计
| 在上述理论的指导下,本节采用了体现学生主体地位的“问题—探究—讨论—总结—应用”的教学方式。即教师通过能源问题引出思维探究,经讨论、总结得出盖斯定律,并应用巩固。
|
教学环节
| 教 学 内 容
| 设计意图
|
| 教师活动设计
| 学生活动设计
| |
引入新课
| [教师]下列数据表示燃烧热吗?
H2(g)+1/2O2(g)==H2O(g) △H1=-241.8kJ/mol
那么,H2的燃烧热△H究竟是多少?
已知: H2O(g)==H2O(l) △H2=-44kJ/mol
如何测出这个反应的反应热:C(s)+1/2O2(g)==CO(g) ΔH1=?
思考并回答:①能直接测出吗?如何测?
②若不能直接测出,怎么办?
得出方案:
①C(s)+1/2O2(g)==CO(g) ΔH1=?
②CO(g)+1/2O2(g)== CO2(g) ΔH2=-283.0kJ/mol
③C(s)+O2(g)==CO2(g) ΔH3=-393.5kJ/mol
① + ② = ③ ,
则 ΔH1 + ΔH2 =ΔH3
所以,ΔH1 =ΔH3-ΔH2 =-393.5kJ/mol+ 283.0kJ/mol=-110.5kJ/mol
为什么可以这样计算?应用了什么原理?
| 不是,因为当水为液态是反应热才是燃烧热。
H2(g)+1/2O2(g)==H2O(l) △H=△H1+△H2=-285.8kJ/mol
| 与旧知识“燃烧热”相衔接,减少学生的陌生感,且为学生设计测定“C(s)+1/2O2(g)==CO(g) ΔH1=?”做好知识与理解的铺垫。
使学生首先在无意识的情况下应用盖斯定律,以便对盖斯定律的理解。
|
导学达标
| 三、盖斯定律
不管化学反应是分一步完成或分几步完成,其反应热是相同的。换句话说,化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。这就是盖斯定律。
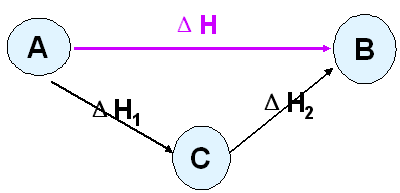
四、对盖斯定律的理解与分析
请观察思考:ΔH、ΔH1、ΔH2之间有何关系?
根据能量守恒定律引导学生理解盖斯定律
|
学生理解
ΔH=ΔH1+ΔH2
| 培养学生认知能力
|
导学达标
| 石墨能直接变成金刚石吗?
例1:写出石墨变成金刚石的热化学方程式(25℃,101kPa时)
说明: (1)可以在书中查找需要的数据
(2)并告诉大家你设计的理由。
①C(石墨,s)+O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(金,s)+O2(g)=CO2(g) △H2=-395.0kJ/mol
所以, ①- ②得:
C(石墨,s)= C(金刚石,s) △H=+1.5kJ/mol
这个热化学方程式说明了什么?
题型一: 已知一定量的物质参加反应放出的热量,计算反应热,写出其热化学反应方程式。
例1、将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为_____________。又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_____________kJ。
题型二:利用盖斯定律求反应热
例2、科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。
(1)P4(s,白磷)+5O2=P4O5(s)
△H1=-2983.2KJ/mol
(2)P(s,红磷)+5/4O2(g)=1/4P4O10(s)
△H2=-738.5KJ/mol
则白磷转化为红磷的热化学方程式 _____ 。相同的状况下,能量较低的是________;白磷的稳定性比红磷_________(填“高”或“低”)。
题型三:根据一定量的物质参加反应放出的热量(或根据已知的热化学方程式),进行有关反应热的计算或比较大小。
| 查阅燃烧热数据,设计方案
石墨不会自动变成金刚石;石墨与金刚石的能量相差不远
| 培养学生的提出问题的解决问题的能力以及计算能力
让学生学会盖斯定律人相关计算
|
导学达标
| 例3、已知下列两个热化学方程式:
H2 (g) +1/2O2(g)==H2O (l) H=285.8 kJ·mol1
C3H8(g)+5O2(g) == 3CO2(g) +4H2O (l) H=2220.0 kJ·mol1
实验测得氢气和丙烷的混合气体共5 mol,完全燃烧时放热3847kJ,则混合气体中氢气和丙烷的体积比是_______,两者放出的热量之比约为_____
A、1:3 B、3:1 C、1:4 D、5:13
解法一:十字交叉法
解法二:估算排除法
答案:BD
题型四:反应热大小比较
题型五:利用键能计算反应热方法:ΔH=∑E(反应物)-∑E(生成物),即反应热等于反应物的键能总和跟生成物的键能总和之差。常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能常用E表示,单位是kJ/mol。 例5.CH3—CH3→CH2=CH2+H2;有关化学键的键能如下。化学键 C-H C=C C-C H-H键能(kJ/mol) 414.4 615.3 347.4 435.3
试计算该反应的反应热
| 解题
解题
解题
| 培养学生解决问题的能力
|
作业
设计
| |
板书设计
| 三、盖斯定律
应用盖斯定律计算反应热
题型一: 已知一定量的物质参加反应放出的热量,计算反应热,写出其热化学反应方程式。
题型二:利用盖斯定律求反应热
题型三:根据一定量的物质参加反应放出的热量(或根据已知的热化学方程式),进行有关反应热的计算或比较大小
题型四:反应热大小比较
题型五:利用键能计算反应热
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图