课题
| 第四章 化学反应与电能
第一节 原电池
第一课时
|
教学目标
| 知识与技能
| 1、复习原电池的化学原理,掌握形成原电池的基本条件。
2、常识性介绍日常生活中常用的化学电源。并能从电极反应的角度认识常见电源的化学原理
|
| 过程与方法
| - 通过拆分干电池和学会自制简易电池培养学生观察能力与分析
思维能力,并通过了解电池的化学组成而增强环保意识。
2、通过化学化学电源的使用史实引导学生以问题为中心的学习方法。学会发现问题、解决问题的方法。加深理解实践→认识→再实践→再认识的辨证唯物主义的思维方法
|
| 情感态度
与价值观
| - 通过原电池的发明、发展史,培养学生实事求是勇于创新的科学
态度。
2、激发学生的学习兴趣与投身科学追求真理的积极情感。
|
教学
重点
| 电极反应的书写
|
教学
难点
| 电极反应的书写
|
教 学 设 想
| 教材分析
| 本节课是对原电池原理的应用,同时了解生活实际,有利于用化学知识来解决生活中的实际问题
|
| 学情分析
| 学生已经学了氧化还原反应的理论和原电池知识,为学习化学电源做了思想上和能力上的准备。 对原电池的工作原理有神秘感和探索欲望。要充分利用学生的好奇心和求知欲,设计层层实验和问题情境,使学生在自主实验、积极思考和相互讨论中自己发现问题、分析问题和解决问题。
|
教学环节
| 教 学 内 容
| 设计意图
|
| 教师活动
| 学生活动
| |
引入新课
| 【提问】
组成原电池的条件:
①有两种活动性不同的金属(或一种是非金属导体)作电极
②电极均插入电解质溶液中
③两极相连形成闭合回路
立即用多媒体展示相应的原电池图片,使学生的认识直观、清晰。
再很自然地引出利用原电池的原理我们已经制作使用的化学电池。
【引课】第二节 化学电源
1、一次电池
一次电池的活性物质(发生 氧化还原反应的物质)消耗到一定程度,就不能再使用了。如普通的 锌锰干电池 、 碱性锌锰电池 、锂电池、锌银电池等都是一次电池。
1)普通锌锰干电池的电极反应和总反应分别为:
负极:
正极: 2NH4+ + 2MnO2 + 2eˉ ══ Mn2O3 + 2NH3↑ + H2O
总反应:Zn + 2NH4+ + 2MnO2 ══Zn2+ + Mn2O3 + 2NH3↑ + H2O
2)碱性锌锰电池(Zn|KOH|MnO2)的电极反应和总反应分别为:
负极:
正极: 2MnO2 + 2H2O + 2eˉ ══ 2MnOOH + 2OHˉ
总反应:Zn + 2MnO2 + 2H2O ══ 2MnOOH + Zn(OH) 2
特点:必能量和可存储时间均有提高, 适用于大电流和连续放电
3)锂电池 负极:
电池特点:质轻、高能(比能量高)、高工作效率、高稳定电压、工作温度宽、高使用寿命,广泛应用于军事和航空领域。
4)锌银电池 (电解液KOH溶液)
负极( Zn ): Zn - 2eˉ+ 2OHˉ== Zn(OH)2
正极(Ag2O):Ag2O +2eˉ+H2O ═2Ag+ 2OHˉ
总反应: Zn + Ag2O +H2O ═2Ag + Zn(OH)2
特点:比能量大、电压稳定、储存时间长、适宜小电流连续放电。
| 书写
记忆
理解
| 复习引入新课
让学生在原电池学习的基础上进一步书写电极反应
|
导学达标
| 2、二次电池
 二次电池又称充电电池或蓄电池,放电后可以再充电,使活性物质获得
二次电池又称充电电池或蓄电池,放电后可以再充电,使活性物质获得
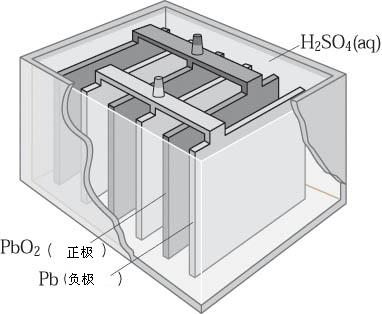
再生,恢复工作能力,实现电池的多次重复使用。最典型的为铅蓄电池,
铅蓄电池放电时的电极反应和总反应分别为:(电解液H2SO4溶液)
负极(Pb): Pb -2eˉ + SO42ˉ═PbSO4
正极(PbO2):PbO2 + 2eˉ+4H++ SO42ˉ═PbSO4+2H2O
总反应Pb+PbO2+2H2SO4═2PbSO4+2H2O
铅蓄电池充电时的电极反应和总反应分别为:
阳极:PbSO4 + 2H2O -2eˉPbO2 + 4H+ + SO42ˉ
阴极: PbSO4 + 2eˉ == Pb + SO42ˉ
总反应:2PbSO4 + 2H2O ═ Pb + PbO2 + 2H2SO4
优点:电压稳定、使用方便、安全可靠、价格低廉
缺点:比能量低、笨重,废弃电池污染环境
3、燃料电池——是一种连续地将燃料和氧化剂的化学能直接转化成电能的化学电源又称连续电池
燃料电池的规律:① 燃料通入负极,助燃剂氧气通入正极
② 电极材料一般不参加化学反应,只起传导电子的作用。
燃料电池与前几种电池的差别:① 氧化剂与还原剂在工作时不断补充;
② 反应产物不断排出;③能量转化率高(超过80%),普通的只有30%,有利于节约能源。
1)氢氧燃料电池
(1) 特点: ① 高效、低污染,原料来源广泛
② 电极材料不参加电池反应
(2) 总反应式:2H2 + O2 == 2H2O
负极:2H2 - 4eˉ == 4H+;
正极:O2 + 2H2O + 4eˉ == 4OHˉ
注意:电解质溶液不同,电极反应不同。
当为碱性溶液时:
负极:2H2 + 4OHˉ - 4eˉ== 4H2O
正极:O2 + 2H2O + 4eˉ == 4OHˉ
当为酸性溶液时: 负极:2H2 - 4eˉ == 4H+
正极:O2 + 4H+ + 4eˉ == 2H2O
| 书写
总结
| 通过以上实例,引导学生分析,归纳总结规律,培养学生归纳总结的能力
让学生学以之用,根据已学知识来解决实际问题
让学掌握基本的原电池的电极反应的书写,并学会应用
|
导学达标
| 2)甲烷氢氧燃料电池
当为酸性溶液时:
负极: CH4- 8eˉ + 2H2O == CO2 + 8H+
正极: 2O2 + 8eˉ+ 8H+ == 4H2O
当为碱性溶液时:
负极: CH4- 8eˉ + 10OHˉ == CO32ˉ+ 7H2O 正极: 2O2 + 8eˉ+ 4H2O == 8OHˉ
3)甲醇氢氧燃料电池
当为酸性溶液时:
负极: 2CH3OH - 12eˉ + 2H2O == 2CO2 + 12H+
正极: 3O2 + 12eˉ+ 12H+ == 6H2O
当为碱性溶液时:
负极: 2CH3OH - 12eˉ + 16OHˉ == 2CO32ˉ+ 12H2O 正极: 3O2 + 12eˉ+ 6H2O == 12OHˉ
当电解质为熔融碳酸盐时:
负极: 2CH3OH - 12eˉ+ 6CO32ˉ == 8CO2+ 4H2O
正极: 3O2 + 12eˉ+ 6CO2== 6CO32ˉ
当电解质为固体氧化物时:
负极: 2CH3OH - 12eˉ+ 12O2ˉ == 2CO2+ 4H2O
正极: 3O2 + 12eˉ== 6O2ˉ
| | 培养学生的发散思维,有一定的设计能力
培养学生的归纳总结的能力
培养学生的解决问题的能力
|
作业设计
|
|
板书设计
| 化学电源
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图