|
|
化学中常用的物理量——物质的量
【学习目标】
1.了解物质的量及其单位——摩尔(mol),摩尔质量
2.认识摩尔是物质的量的基本单位,能用于进行简单的化学计算,体会定量研究的方法对研究和学习化学的重要作用
3.了解物质的量、气体摩尔体积、体积之间的关系。
4.通过实验操作学会配制一定物质的量浓度溶液的方法和技能,掌握误差分析的方法。
5.能运用物质的量浓度的概念进行简单计算。
【学习重难点】
1.物质的量及其单位,阿伏加德罗常数以及摩尔质量的定义。
2.物质的量、微粒数、摩尔质量、质量的换算。
3.气体摩尔体积的理解与相关计算。
4.一定物质的量浓度的溶液的配制方法及误差分析,物质的量浓度的理解。
【学习过程】
第一课时
一、物质的量
1.定义
2.符号
3.单位
练习:
1.判断下列说法是否正确?
⑥2mol 蚂蚁; ⑦ 1mol Na+
2.说出下列符合的意义
(1)2H
(2)2molH
(3)2molH+
(4)2molH2
3.计算:
1 mol H2O中含______mol H,______mol 氧原子。
1 mol K2SO4中含______mol 氧原子,______mol 原子。
4.阿伏加德罗常数
(1)规定:1 mol包含个基本单元。这一常数被称为,可以近似表示为,实验表明:阿伏加德罗常数个的质量约为。
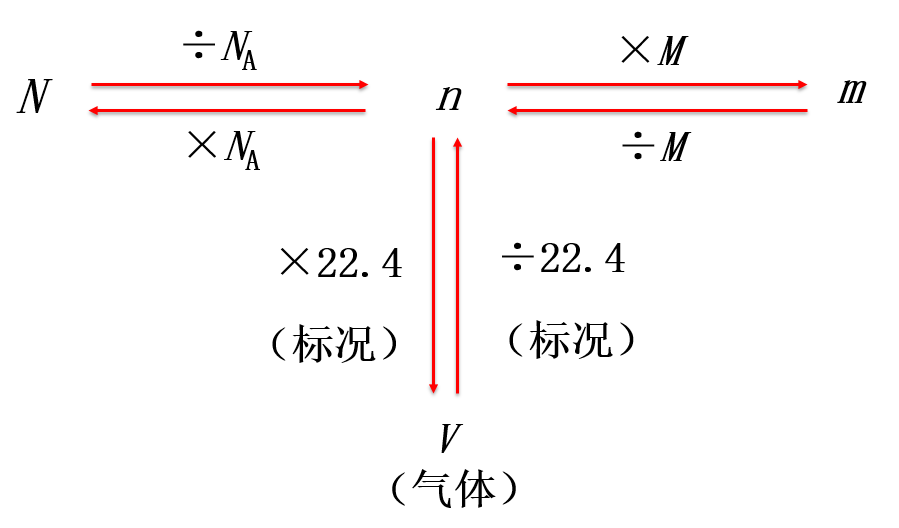
(2)微粒数(N)、阿伏加德罗常数(NA)、物质的量(n)之间的关系
式是。
练习:
(1)1mol O2约含有_____个O2,_____mol O,约含有_____个O。
(2)3mol H2SO4中约含有_____个H2SO4,含有_____mol O,约为_____个O。
(3)2mol NH4+中含有_____mol H,约含有_____个N。
(4)2mol H2O含有_____个H,含有_____个O。
(5)6.02×1023个O2约含有_____molO2,_____mol O。
(6)18.06×1023个H2SO4中约含有_____molH2SO4,含有_____mol O,含有_____mol H。
(7)12.04×1023个NH4+中含有_____mol H,约含有_____个电子。
(8)12.04×1023个H2O含有_____moH,含有_____个O。
三、摩尔质量
1.定义:
2.单位:
3.数值:
练习:填写下列表格
物质
| 分子数
| 质量(g)
| 物质的量(mol)
| 摩尔质量(g/mol)
| 氮气
| | 14
| | | H2SO4
| 3.01×1022
| | | | H2O
| | | 0.5
| |
4.质量(m)、摩尔质量(M)、物质的量(n)之间的关系式是。
练习:
(1)质量相等的下列物质中,含分子数最多的是( )
A.CH4 B.O2 C.NH3 D.CO2
(2)对于同质量的二氧化硫和三氧化硫来说,下列关系中正确的是( )
A.含氧原子的个数比为2∶3
B.含硫元素的质量比为5∶4
C.含氧元素的质量比为6∶5
D含硫原子的个数比为1∶1
(3)①等物质的量O2和臭氧(O3),所含的分子数之比为,所含的氧原子数之比为,其分子量之比为,其质量之比为。
②若O2和O3质量相等,则其分子数之比为,氧原子数之比为。
小结:
第二课时
科学探究:请计算是1mol物质在0℃、1.01×105Pa下的体积
物质
| 状态
| 质量(g)
| 密度 (g/cm3)
| 体积
| Fe
| 固
态
| 55.8
| 7.88
|
| Al
| | 26.98
| 2.7
|
| Pb
| | 207.2
| 11.3
|
| H2O
| 液
态
| 18
| 1
|
| H2SO4
| | 98
| 1.83
|
| H2
| 气
态
| 2.016
| 0.0899 g/ L
|
| O2
| | 32
| 1.43 g/ L
|
| CO2
| | 44.01
| 1.977 g/ L
|
|
思考:
1.为什么1mol不同状态的物质体积不同;
2.为什么1mol不同物质的气体体积近似相等,且比固、液物质体积大的多;
3.影响物质体积的因素究竟是什么?
一、影响物质体积的因素
1.影响物质体积的因素
(1)构成物质的粒子________;(2)粒子的________;(3)_______________。
2.影响固体或液体体积的主要因素
① ②
3.决定气体体积的主要因素
① ②
二、气体摩尔体积
1.概念:
2.符号:
3.定义式:
4.单位:
5.气体在标准状况下的摩尔体积约是22.4L。
练习:判断正误
(1)在标准状况下,1 mol任何物质的体积都约为22.4 L。
(2)1 mol气体的体积约为22.4 L。
(3)在标准状况下,1 mol O2和N2混合气(任意比)的体积约为22.4 L。
(4)22.4 L气体所含分子数一定大于11.2 L气体所含的分子数。
(5)任何条件下,气体的摩尔体积都是22.4 L。
(6)只有在标准状况下,气体的摩尔体积才能是22.4 L。
6.注意事项:
①条件:
②研究对象:
③物质的量:
④所占体积:
练习:
(1)在标准状况下,2.2 g CO2 的体积是多少?
(2)标准状况下,112 mL 某气体的质量为0.14 g,则其摩尔质量为_______________,相对分子质量为___________。
小结:
第三课时
一、配制一定物质的量浓度的溶液
1.步骤
①计算:。
②称量:。
思考:称量时能将NaCl固体直接放置于托盘上吗?
③溶解:将溶质倒入小烧杯,加入适量的水搅拌溶解,冷却致室温.
④冷却:冷却至室温
方法导引:认识容量瓶
构造:形的平底玻璃瓶,瓶口配有 。
特点:①容量瓶上标有②容量瓶瓶颈处有
用途:用于配制的溶液
注意事项:
①使用前要检查是否漏水
②不能在容量瓶中进行溶解或稀释操作
③不能用做反应容器或长期存放溶液
⑤转移和洗涤:将上述冷却后的溶液 转入,并用蒸馏水洗涤小烧杯和玻璃棒次,将洗涤液一并注入容量瓶。
思考:
(1)如何将烧杯中的液体转移到容量瓶中
(2)为什么要洗涤玻璃棒和烧杯?
⑥定容:在容量瓶中继续加水至距刻度线cm处,改用滴加至刻度(液体与刻度线相切)。
思考:如果仰视或者俯视刻度线对溶液体积有何影响?
⑦摇匀:把定容好的容量瓶瓶塞塞紧,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动几次,混合均匀。
⑧装瓶贴签:(容量瓶不能保存溶液)
小结:
计算→称量→溶解→冷却→转移→洗涤→定容→摇匀→装瓶贴签
思考:通过上述对实验过程的探究请总结在实验过程中用的仪器。
2.所用仪器:
思考:在配制过程中由于操作不当,会引起误差,那么这些错误当操作会对实验结果有什么影响呢?请同学们认真思考。
3.误差分析:
(1)称量产生误差
①称量时左盘高,右盘低
②称量时称量物放在右盘,而砝码放在左盘
(2)溶解、转移、洗涤产生误差
③溶解过程中有少量液体溅出烧杯
④未洗涤溶解用的玻璃棒和烧杯
⑤洗涤液未转入容量瓶中
(3)定容误差
⑥定容时仰视刻度
⑦定容时俯视刻度
⑧定容时液面低于刻度线
⑨未等溶液冷却就定容
⑩摇匀后发现液面低于刻度再加水
二、物质的量浓度
指导阅读:思考什么是物质的量浓度
1.定义:
2.单位:
3.公式:
练习巩固:
1.用40gNaOH配成2L溶液,其物质的量浓度________mol/L
2.58.5gNaCl配成500mL溶液,其物质的量浓度________mol/L
3.根据物质的量浓度的概念判断下列说法是否正确:
A.将40gNaOH溶于1L水中,所得溶液的物质的量浓度为1 mol/L;
B.将98g硫酸溶液稀释配成1L溶液,所得溶液的物质的量浓度为1 mol/L;
迁移应用:
(1)为了测定某废水中硫酸的总量,某化学兴趣小组取100 mL废水样品注入烧杯中,测定后得知H2SO4 的物质的量浓度为1.5mol • L -1,然后通过该物质的量浓度和废水的总体积计算出废水中硫酸的总量。该兴趣小组的做法给了你怎样的启示?
(2)将2mol Na2SO4溶于水,配成4L溶液,CNa2SO4=
(3)配制2mol·L-1 NaCl溶液100ml,则NaCl的物质的量=,NaCl的质量=。
交流研讨:
在实验室里需要制取一定量的氢气。现将0.65g金属锌放入一定体积的2mol∙L-1的盐酸中,它们恰好完全反应。请完成下面的表格。
化学反应
| Zn + 2HCl===ZnCl2 + H2↑
| 物质的量
|
|
|
|
| 质量或气体体(STP)
| 0.65g
|
|
|
|
讨论:
(1)分别用质量、物质的量计算所需盐酸的体积。比较使用哪种物理量进行计算更方, 更能反映出宏观物质之间进行反应时微观粒子之间的数量关系。
(2)学习了物质的量这一物理量后,你对化学反应中的定量关系有了哪些新的认识?
【检测反馈】
第一课时
1.下列叙述正确的是( )
A.每摩尔物质约含有6.02×1023个粒子 B.摩尔是七个基本物理量之一
C.摩尔是物质的质量单位 D.摩尔是物质的数量单位
2.下列关于物质的量的说法中正确的是( )
A.物质的量是国际单位制中的七个基本物理量之一
B.物质的量实质上就是物质的质量
C.物质的量是一种物理量的单位
D.摩尔既是物质的量的单位,又是粒子数量的单位
3.在0.6 mol Ba(OH)2中,含有OH-的数目是( )
A.约为1.2 B.约为7.22×1023
C.约为6.02×1023 D.约为3.01×1023
4.设NA表示阿伏加德罗常数,下列说法正确的是( )
A.1 mol氦气中有2NA个氦原子 B.使用摩尔时必须指明粒子的名称
C.1 mol任何物质所含的原子数为NA个 D.1 mol任何物质所含的粒子数为NA个
5.同质量的下列气体中,所含原子数最少的是( )
A.CH4 B.CO2 C.H2S D.N2
6.下列关于阿伏加德罗常数的说法正确的是( )
A.阿伏加德罗常数是12 g碳中所含的碳原子数
B.阿伏加德罗常数是0.012 kg 12C中所含的原子数
C.阿伏加德罗常数是6.02×1023
D.阿伏加德罗常数的符号为NA,近似为6.02×1023
7.下列叙述中正确的是( )
A.1 mol任何纯净物都含有相同的原子数
B.1 mol O2中约含有6.02×1023个氧气分子
C.1 mol氢中含有2 mol氢原子
D.阿伏加德罗常数就是6.02×1023
8.下列关于摩尔的认识,正确的是( )
A.摩尔是表示微观粒子多少的物理量
B.摩尔是物质的量的单位
C.摩尔是粒子数与阿伏加德罗常数之比
D.摩尔是描述宏观物质多少的单位
9.下列对阿伏加德罗常数的叙述中,正确的是( )
①阿伏加德罗常数就是6.02×1023 mol-1 ②阿伏加德罗常数为1 mol指定粒子的粒子数 ③阿伏加德罗常数为12 g 碳所含的碳原子数 ④阿伏加德罗常数用符号NA表示,其值约为6.02×1023 mol-1
A.①② B.①③ C.②③ D.②④
10.1 g CO中含a个原子,则阿伏加德罗常数可以表示为( )
C.14a mol-1 D.28a mol-1
11.下列关于物质的量的叙述中,正确的是( )
A.1 mol 任何物质都含有6.02×1023个分子
B.0.012 kg 14C中约含有6.02×1023个碳原子
C.1 mol水中含有2 mol氢和1 mol氧
D.1 mol Ne 约含有6.02×1024个电子
12.(1)0.3 mol NH3分子中所含原子数与________个H2O分子中所含原子数相等。
13.(1)1 mol O原子中约含有________个O原子。
(2)3 mol H2SO4中约含有________个H2SO4,约含有________个H原子,约含有________个O原子。
(3)4 mol O2含有______ mol O原子。
(4)6.02×1024个Na+物质的量约为______mol。
参考答案
1.A 2.A 3.B 4.B
5.B 6.B 7.B 8.B 9.D 10.C 11.D
12.(1)2.408×1023 (2)0.6 mol
13.(1)6.02×1023 (2)1.806×1024 3.612×1024 7.224×1024 (3)8 (4)10
第二课时
1.当温度和压强一定时,决定气体体积大小的主要因素是( )
A.分子直径的大小 B.分子间距离的大小
C.分子间引力的大小 D.分子数目的多少
2.下列有关气体摩尔体积的描述中正确的是( )
A.相同物质的量的气体摩尔体积也相同
B.通常状况下的气体摩尔体积约为22.4 L
C.标准状况下的气体摩尔体积约为22.4 L·mol-1
D.一定物质的量的气体所占的体积就是气体摩尔体积
3.在标准状况下,由0.5 g H2、11 g CO2和4 g O2组成的混合气体,其体积约为( )
A.8.4 L B.11.2 L C.14.0 L D.16.8 L
4.在标准状况下,与12 g H2的体积相等的N2( )
A.质量为12 g B.物质的量为6 mol C.体积约为22.4 L D.分子数约为6.02×1023
5.下列说法正确的是( )
A.标准状况下,6.02×1023个分子所占的体积约是22.4 L
B.0.5 mol H2所占的体积是11.2 L
C.标准状况下,1 mol H2O的体积为22.4 L
D.标准状况下,28 g CO与N2的混合气体的体积约为22.4 L
6.下列两种气体的分子数一定相等的是( )
A.质量相等的N2和CO B.体积相等的CO和C2H4
C.等温、等体积的O2和N2 D.等压、等体积的N2和CO2
7.相同条件下,等物质的量的两种气体一定满足( )
A.体积均为22.4 L B.具有相同的体积
C.是双原子组成的分子 D.所含原子数目相同
8.阿伏加德罗常数约为6.02×1023 mol-1,下列说法一定正确的是( )
A.22.4 L N2中所含的分子个数为6.02×1023
B.标准状况下,22.4 L Cl2和HCl的混合气体中含分子总数为2×6.02×1023
C.4℃时,22.4 L水含水分子数为6.02×1023
D.20 g Ne含原子个数为6.02×1023
9.下列物质中,含氢原子数目最多的是( )
A.0.9 mol H2O B.0.3 mol H2SO4 C.0.2 mol NH3 D.0.4 mol CH4
10.在同温同压下,某瓶充满O2时质量为116 g,充满CO2时质量为122 g,充满气体X时质量为114 g,则X的相对分子质量为( )
A.28 B.60 C.32 D.44
11.在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g。则两种气体的物质的量之和为________mol,其中CO2为________mol,CO占总体积的________%。
参考答案
1.D 2.C 3.C 4.B 5.D 6.A 7.B 8.D 9.A 10.A
11.1.75 0.75 57.1
第三课时
一、选择题
1.在容量瓶上无需标记的是( )
A.刻度线 B.温度 C.浓度 D.容量
2.下列溶液中,溶质的物质的量浓度为1 mol·L-1的是( )
A.将40 g NaOH溶于1 L水所得的溶液
B.将22.4 L HCl溶于水配成1 L溶液
C.1 L 含2 mol K+的K2SO4
D.将0.5 mol·L-1的NaNO3溶液100 mL 加热蒸发掉50 g水后的溶液
3.下列溶液中的c(Cl-)与50 mL 1 mol·L-1 AlCl3溶液中的c(Cl-)不相等的是( )
A.150 mL 1 mol·L-1氯化钠溶液 B.75 mL 1.5 mol·L-1氯化钙溶液
C.150 mL 3 mol·L-1氯化钾溶液 D.75 mL 1 mol·L-1氯化铁溶液
4.下列说法中,正确的是( )
A.在1 L水中溶解58.5 g NaCl固体,则该溶液的物质的量浓度是1 mol·L-1
B.从1 L 2 mol·L-1的H2SO4溶液中取出0.5 L,则取出溶液的物质的量浓度是
1 mol·L-1
C.配制500 mL 0.5 mol·L-1的CuSO4溶液时,需要62.5 g CuSO4·5H2O晶体
D.中和100 mL 1 mol·L-1的H2SO4溶液时,需要NaOH的质量是4 g
5.如图是某溶液在稀释过程中,溶质的物质的量浓度随溶液体积的变化曲线图,根据图中的数据分析得出V值等于( )
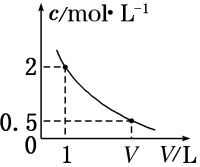
A.2 B.3 C.4 D.5
6.把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为( )
A.0.1(b-2a)mol·L-1 B.10(2a-b)mol·L-1
C.10(b-a)mol·L-1 D.10(b-2a)mol·L-1
7.20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是( )
A.25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
C.20℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20 ℃时,溶液密度一定大于1.174 g·cm-3
8.11.2 g Fe与500 mL 2 mol·L-1的盐酸反应,生成标准状况下H2的体积为( )
A.11.2 L B.2.24 L C.4.48 L D.3.36 L
9.下列各溶液中,Na+浓度最大的是( )
A.4 L 0.5 mol·L-1NaCl溶液 B.1 L 0.3 mol·L-1Na2SO4溶液
C.0.8 L 0.4 mol·L-1NaOH溶液 D.2 L 0.15 mol·L-1Na3PO4溶液
11.欲配制100 mL 1.0 mol·L-1Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4溶于100 mL水中
②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL
③将20 mL 5.0 mol·L-1Na2SO4溶液用水稀释至100 mL
A.①② B.②③ C.①③ D.①②③
A.0.20 mol·L-1 B.0.25 mol·L-1 C.0.40 mol·L-1 D.0.50 mol·L-1
13.实验室用氯化钠固体配制1.00 mol·L-1的NaCl溶液0.5 L,回答下列问题:
(1)请写出该实验的实验步骤:
①__________;②__________;③__________;④__________;⑤__________;⑥__________。
(2)所需仪器为:容量瓶(规格:_______________)、托盘天平,还需要哪些实验仪器才能完成该实验,请写出:。
(3)试分析下列操作对所配溶液的浓度的影响及造成该影响的原因。
①为加速固体溶解,可稍微加热并不断搅拌。固体全部溶解后,立即将溶液转移至容量瓶定容,使所配溶液浓度________,原因是_________________________________________。
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线,使所配溶液浓度________,原因是____________________________。
14.过氧化钠能与水发生反应,某同学欲用该反应制取标准状况下的氧气1.12 L。
(1)计算至少需要称取过氧化钠的质量为________。
(2)若反应所得氢氧化钠溶液的体积是200 mL ,计算该溶液中溶质的物质的量浓度为________。
参考答案:
1-5 C C A C C 6-10 D D C B D 11-12 B C
(2)500 mL 烧杯、药匙、玻璃棒、胶头滴管
(3)①偏高 恢复到室温时,溶液的体积将小于500 mL ②偏低 溶液体积大于500 mL
14.(1)7.8 g (2)1 mol·L-1
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图