|
|
2.2.1化学反应中能量变化的本质及转化形式

1.了解化学反应中化学能与热能的相互转化,了解吸热反应、放热反应,熟悉常见的放热反应与吸热反应。
2. 认识化学反应中能量变化的实质,能从微观和宏观两个角度认识化学反应伴随能量变化的原因。

化学反应伴随能量变化的原因

1.化学键是;
称为离子键,称为共价键键。
2.化学反应的实质;需要吸收能量,
会释放能量。

【回顾思考】
1.如何区分化学变化和物理变化?化学反应的实质是什么?
2.前面我们学过了哪些类型的化学反应?这些反应都有什么特征?
3.现实生活中我们是如何利用化学反应的?
【联想质疑】
1.木炭燃烧反应方程式,能量变化能转化为。
2.电解水反应方程式,能量变化能转化为。
一、化学反应中能量变化的本质及转化形式
1.吸热反应与放热反应
化学反应的实质是旧化学键的断裂和新化学键的形成。旧化学键断裂吸收能量,新化学键形成释放能量。化学反应中不仅有物质变化还伴随着。
【活动探究】根据教材“活动探究”所给用品小组合作设计实验方案并进行实验,感受化学反应中的能量变化。完成表格。
总结:吸热反应:
放热反应:
常见的放热反应:。
常见的吸热反应:。
2.化学反应中能量变化的原因分析
【交流研讨】完成教材P48页“交流·研讨”,通过计算判断反应过程吸热和放热情况,并从化学键的角度分析化学反应中能量变化的实质。
断裂化学键吸收的总能量=
形成化学键放出的总能量=
生成1mol水的能量
【总结】
(1)从化学键的角度分析化学反应中能量变化
断裂化学键吸收的能量为E1 形成化学键释放的能量E2 反应释放能量(放热反应)
断裂化学键吸收的能量为E1形成化学键释放的能量E2 反应吸收能量(吸热热反应)
【自主学习】阅读教材P48页最后一段,了解化学反应能量变化与物质能量的关系。
(2)从物质内部能量的角度分析化学反应中能量变化
反应物所具有的总能量 生成物所具有的总能量 反应释放能量(放热反应)
反应物所具有的总能量生成物所具有的总能量 反应吸收能量(吸热热反应)
【迁移应用】古诗《石灰吟》:千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间。是一首托物言志诗。作者以石灰作比喻,表达自己为国尽忠,不怕牺牲的意愿和坚守高洁的决心。通过古诗的描述,写出有关的方程式,并判断制取石灰的反应是放热反应还是吸热反应?石灰遇水的反应呢?
3.化学反应中能量转化的形式
利用化学反应将化学能转化为、等其他形式的能量,用于生产、
生活和科研。化学家也常常利用热、等促使很多化学反应发生,获得所需要的物质。

1.物质在发生化学变化时,下列说法正确的是( )
A.反应物的总质量等于生成物的总质量
B.发生电子得失或偏移
C.有化学键的断裂,不一定有新物质生成
D.反应物所具有的总能量等于生成物所具有的总能量
2.下列说法正确的是( )
A.物质发生化学反应时都伴随着能量变化
B.伴有能量变化的物质变化都是化学变化
C.在一个确定的化学反应体系中,反应物的总能量与生成物的总能量一定相同
D.在一个确定的化学反应体系中,反应物的总能量总是高于生成物的总能量
3.下列说法正确的是( )
A.任何化学反应都伴随着能量的变化
B.H2O(g)===H2O(l)该过程放出大量的热,所以该过程是化学变化
C.化学反应中能量的变化都表现为热量的变化
D.对于如图所示的过程,是吸收能量的过程
4.下图表示化学反应过程中的能量变化,据图判断下列说法中合理的是( )
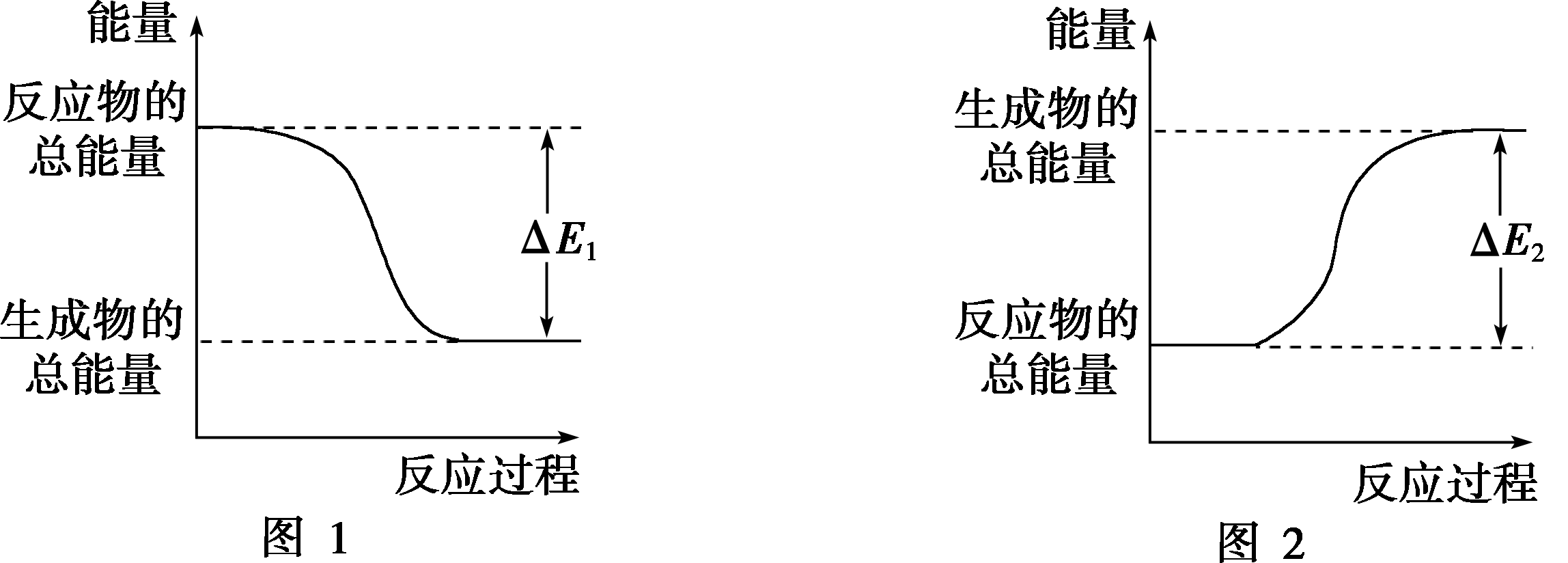
A.500 mL 2.0 mol·L-1 HCl和500 mL 2.0 mol·L-1NaOH的反应符合图1,且放出热量为ΔE1
B.500 mL 2.0 mol·L-1 H2SO4和500 mL 2.0 mol·L-1Ba(OH)2的反应符合图2,且吸收热量为ΔE2
C.发生图1能量变化的任何反应,一定不需要加热即可发生
D.CaO、浓硫酸分别溶于水时的能量变化符合图1
5.下列变化一定为放热反应的是( )
A.1 mol气态水变为1 mol液态水放出44 kJ的热量
B.2HI(g) H2(g)+I2(g),生成1 mol I2需要吸收14.9 kJ的能量
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如图所示的化学反应:
6.研究物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及能量变化。据此判断以下叙述中错误的是( )
A.金属钠与氯气反应生成氯化钠后,其结构的稳定性增强,体系的能量降低
B.物质燃烧可看作是储存在物质内部的能量(化学能)转化为热能释放出来
C.氮气分子内部存在着很强的化学键,故通常情况下氮气的化学性质很活泼
D.需要加热才能发生的反应不一定是吸收能量的反应
7.(1)在1 mol氢分子中,含有________mol氢原子,含有________mol H—H键。
(2)已知在25 ℃和101 kPa条件下,由2 mol H原子形成1 mol H—H键时,放出436 kJ的能量。若要使1 mol氢分子变为2 mol氢原子时,需要断开1 mol H—H键,其能量变化是__________。
(3)在CH4中,断开1 mol C—H键要吸收415 kJ的能量。若要形成1 mol CH4中的C—H键其能量变化是________________。
8.断开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要吸收的能量为436 kJ、391 kJ、946 kJ。
(1)1 mol N2完全反应生成NH3需________(填“吸收”或“放出”)能量________kJ。
(2)1 mol H2完全反应生成NH3需________(填“吸收”或“放出”)能量________kJ。(不考虑可逆反应)
检测反馈答案
1.【答案】A
【解析】 A项符合质量守恒,正确;非氧化还原反应没有电子得失或偏移,B项不正确;化学变化时有化学键的断裂,则一定有新物质生成,C项不正确。
2.【答案】 A
【解析】 物质发生化学反应时都伴随着能量变化,伴有能量变化的物质变化不一定是化学变化,如物质发生核变(如原子弹的爆炸)时也伴有能量变化。在一个确定的化学反应体系中,反应物的总能量(设为x)与生成物的总能量(设为y)之间的关系:①x>y,化学反应为放热反应;②x<y,化学反应为吸热反应。
3.【答案】 A
【解析】 任何化学反应都有能量的变化,但有能量变化的过程不一定是化学变化,如物质的三态变化,虽然存在能量变化,但不存在旧化学键的断裂与新化学键的形成,故不是化学变化,所以A项正确,B项错误;化学反应中能量变化的形式有多种,除热能外,还有光能、电能等,C项错误;由图像知,该过程中反应物的总能量大于生成物的总能量,故该过程中放出了能量,D项错误。
4.【答案】A
【解析】图1表示放热反应,选项A是放热反应,故正确;图2表示吸热反应,选项B是放热反应,故错误;选项C,一些放热反应需加热才能发生,故错误;选项D,浓硫酸溶于水虽然会放出热量,但不属于化学反应,故错误。
5.【答案】D
【解析】A项,H2O(g)===H2O(l)不是化学反应;B项中的反应为吸热反应;如果断裂化学键时吸收的能量比862 kJ多,则反应为吸热反应,反之为放热反应,故C项不一定为放热反应;反应物总能量高于生成物总能量的化学反应一定是放热反应,D正确。
6.【答案】 C
【解析】氮气分子内部存在很强的化学键,故通常情况下氮气的化学性质很不活泼。
7.【答案】 (1)2 1 (2)吸收436 kJ的能量 (3)放出4 mol×415 kJ·mol-1=1 660 kJ的能量
8.【答案】(1)放出 92 (2)放出 30.67
【解析】本题可以从断键吸收的能量数值与成键放出的能量数值的相对大小来判断,若E(断键)>E(成键),
则为吸热反应;若E(断键)<E(成键),则为放热反应。(1)N2+3H22NH3,生成2 mol NH3形成6 mol N—H键时要放出6 mol×391 kJ·mol-1=2 346 kJ的能量,拆开1 mol N≡N键和3 mol H—H键时吸收的总能量为中的能量变化为放出能量,为 2346 kJ-2 254 kJ=92 kJ。(2)由(1)知3 mol H2生成NH3需放出能量92 kJ,则1 mol H2生成NH3需放出能量为92 kJ×1/3 ≈30.67 kJ。
|
|
![]() 川公网安备51152402000101号 )|网站地图
川公网安备51152402000101号 )|网站地图